
在密闭容器中进行如下反应:H2(g)+I2(g)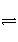
 2HI(g)。在温度T1和T2时,产物的量与反应时间的关系如图所示。符合图所示的正确判断是( )
2HI(g)。在温度T1和T2时,产物的量与反应时间的关系如图所示。符合图所示的正确判断是( )
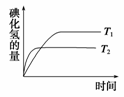
A.T1>T2,ΔH>0 B.T1>T2,ΔH<0
C.T1<T2,ΔH>0 D.T1<T2,ΔH<0
科目:高中化学 来源: 题型:
利用如图装置测定中和热的实验步骤如下:
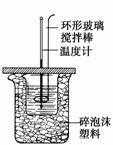
①用量筒量取50 mL 0.25 mol·L-1硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50 mL 0.55 mol·L-1 NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3 kJ·mol-1):________________________________________________________________________
________________________________________________________________________。
(2)倒入NaOH溶液的正确操作是______(从下列选出)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使硫酸与NaOH溶液混合均匀的正确操作是______(从下列选出)。
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(4)实验数据如下表:
①请填写下表中的空白:
| 温度 实验次数 | 起始温度t1℃ | 终止温 度t2/℃ | 温度差平均值(t2-t1) /℃ | |
| H2SO4 | NaOH | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 |
②近似认为0.55 mol·L-1 NaOH溶液和0.25 mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18 J·g-1·℃-1。则中和热ΔH=
________________________________________________________________________
( 取小数点后一位)。
③上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是(填字母)
____________。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
诺贝尔化学奖获得者施罗克等人发现,金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为
①2MoS2+7O2====2MoO3+4SO2;
②MoO3+2NH3·H2O====(NH4)2MoO4+H2O;
③(NH4)2MoO4+2HCl====H2MoO4↓+2NH4Cl;
④H2MoO4 MoO3+H2O;
MoO3+H2O;
⑤用还原剂将MoO3还原成金属钼。
则下列说法正确的是( )
A.反应①和⑤都属于置换反应
B.进行②③④步反应的目的是提纯MoO3
C.在反应①中Mo和S均被氧化
D.利用H2、CO和铝分别还原等量的MoO3,消耗还原剂的物质的量之比为2∶2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机化合物的说法正确的是 ( )
A.乙酸和乙酸乙酯可用Na2CO3溶液加以区别
B.戊烷(C5H12)有两种同分异构体
C.乙烯、聚氯乙烯和苯分子中均含有碳碳双键
D.糖类、油脂和蛋白质均可发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)元素甲是第3周期ⅦA族元素,甲元素与另两种非金属元素可组成离子化合物A。写出A的化学式 ,A中含有的化学键是 。
(2)在第3周期元素的气态氢化物中,元素乙的氢化物最稳定,写出元素乙的单质与水反应的化学方程式 。
(3)金属元素丙形成的某化合物的溶液常用于检验CO2,则元素丙的简单离子与
元素甲的简单离子的半径大小关系是 (用离子符号表示),
元素丁的原子序数比丙小8,写出元素丁的单质在CO2中燃烧的化学方程式
。
(4)元素戊是第3周期中简单离子半径最小的元素,写出该元素的最高价氧化物对应水化物与NaOH溶液反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列有关图象,说法正确的是( )
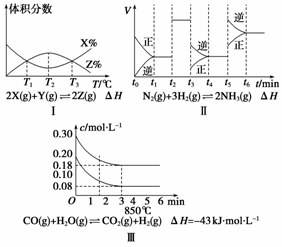
A.由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的ΔH<0
B.由图Ⅱ知,反应在t6时刻,NH3体积分数最大
C.由图Ⅱ知,t3时采取了增大反应体系压强的措施
D.图Ⅲ表示在10 L容器、850℃时的反应,由图知,到4 min时,反应放出51.6 kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列变化不是由加成反应引起的是 ( )
A.苯中加溴水振荡,溴水层褪色
B.烯烃通入溴的CCl4溶液中褪色
C.乙烯在一定条件下生成乙烷
D.苯转化为环己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B属于短周期元素,能以化学键结合成分子式为AB2型的化合物,则B、A元素不可能分别属于周期表中的族数是( )
A.ⅤA和ⅠA族 B.ⅥA和ⅤA族
C.ⅥA和ⅣA族 D.ⅦA和ⅡA族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com