
| A. | 在0.1mol•L-1氨水中加几滴酚酞,再加等体积的醋酸铵溶液,观察红色是否变浅 | |
| B. | 测定0.1 mol•L-1NH4C1溶液的酸碱性 | |
| C. | 测定0.lmol•L-1氨水的pH | |
| D. | 比较浓度均为0.1 mol•L -1的氨水与NaOH溶液的导电能力 |
分析 在水溶液里或熔融状态下部分电离的电解质是弱电解质,如果一水合氨在水溶液里部分电离,则一水合氨是弱电解质,据此分析解答.
解答 解:A.0.1mol/L的氨水能使酚酞试液变红色,说明一水合氨电离出氢氧根离子而使溶液呈碱性,再加等体积的醋酸铵溶液,溶液红色变浅可能说明溶液中存在电离平衡,能证明氨水中一水合氨为弱电解质,也可能是溶液稀释溶液红色变浅,需要加入固体醋酸铵来验证,故A符合;
B.0.1mol/L的氯化铵溶液pH小于7,说明氯化铵是强酸弱碱盐,能说明一水合氨是弱电解质,故B不符合;
C.测定0.lmol•L-1氨水的pH小于13,说明一水合氨在溶液中存在电离平衡,能说明一水合氨为弱电解质,故C不符合;
D.氨水能和氯化亚铁反应生成氢氧化亚铁,说明一水合氨电离出氢氧根离子而使溶液呈碱性,但不能说明一水合氨部分电离,所以不能证明一水合氨是弱电解质,故D不符合;
故选A.
点评 本题考查了强弱电解质的判断,电解质强弱与其电离程度有关,与溶液的酸碱性、导电能力大小无关,为易错点.


科目:高中化学 来源: 题型:实验题

| 序号 | 固体成分(填化学式) |
| 1 | |
| 2 | |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化合物 | 燃烧热 | 化合物 | 燃烧热 |
| 甲烷 | 891.0 | 正丁烷 | 2878.0 |
| 乙烷 | 1560.8 | 异丁烷 | 2869.6 |
| 丙烷 | 2221.5 | 2-甲基丁烷 | 3531.3 |
| A. | 稳定性:正丁烷>异丁烷 | |
| B. | 乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)═4CO2(g)+6H2O(g)△H=-1560.8KJ/mol | |
| C. | 正戊烷的燃烧热大约在3540 KJ/mol左右 | |
| D. | 相同质量的烷烃,碳的质量分数越大,完全燃烧放出的热量越多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-.在含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示.下列说法不正确的是( )
已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-.在含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示.下列说法不正确的是( )| A. | a点反应的离子方程式为 IO3-+3HSO3-=I-+3SO42-+3H+ | |
| B. | b点到c点反应的离子方程式为 IO3-+5I-+6H+=3I2+3H2O | |
| C. | 当溶液中的I-为0.4 mol时,加入的KIO3只能为0.4 mol | |
| D. | 若往100 mL 1mol/L的KIO3溶液中逐滴滴加NaHSO3溶液,反应开始时的离子方程式为 2IO3-+5HSO3-=I2+5SO42-+H2O+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、NO3-、Cl-、Na+ | B. | MnO4-、Ca2+、NO3-、Cl- | ||
| C. | HSO3-、HCO3-、NO3-、SO32- | D. | Na+、Ca2+、NO3-、CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
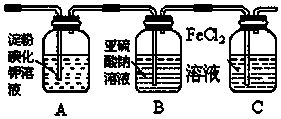
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| Y | Z | ||
| X | W |
| A. | X的最高价氧化物是碱性氧化物 | |
| B. | Z、W均可与Mg形成离子化合物 | |
| C. | 原子半径的大小顺序:r (Z)>r (Y)>r (X) | |
| D. | Y、Z、W的氧化物排放到空气中均会导致酸雨 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com