
【题目】(1)写出氯碱工业电解饱和食盐水的化学方程式:___________________________
(2)已知:2KMnO4 + 16HCl =2KCl+2MnCl2 +5Cl2↑+8H2O,15.8g KMnO4 与100mL12mol/L浓盐酸充分反应,固体完全溶解,生成标准状况下氯气的体积为________L,转移的电子数为_________个,若向反应后的溶液中加入足量的硝酸银,过滤、洗涤、干燥,可得到固体______g。
(3)将标准状况下6.72L的HCl溶于水形成250mL溶液,取出10mL于锥形瓶中,溶质的物 质的量浓度为______mol/L,向锥形瓶中滴加0.5mol/LBa(OH)2溶液,恰好反应,消耗Ba(OH)2的体积为__________mL。
【答案】 2NaCl + 2H2O![]() 2NaOH + H2↑ +Cl2↑ 5.6 0.5NA(或3.01×1023) 100.45 1.2 12
2NaOH + H2↑ +Cl2↑ 5.6 0.5NA(或3.01×1023) 100.45 1.2 12
【解析】(1). 在氯碱工业中,电解饱和食盐水生成NaOH、H2和Cl2,该反应的化学方程式为:2NaCl + 2H2O![]() 2NaOH + H2↑ +Cl2↑,故答案为:2NaCl + 2H2O
2NaOH + H2↑ +Cl2↑,故答案为:2NaCl + 2H2O![]() 2NaOH + H2↑ +Cl2↑;
2NaOH + H2↑ +Cl2↑;
(2). 15.8g KMnO4的物质的量为:15.8g÷158g/mol=0.1mol,与100mL12mol/L浓盐酸充分反应,固体完全溶解,根据反应方程式可知,生成氯气的物质的量为0.1mol×5/2=0.25mol,在标准状况下的体积为0.25mol×22.4L/mol=5.6L,在该反应中,Mn元素的化合价从+7价降低到+2价,所以0.1mol KMnO4完全反应转移电子的物质的量为0.1mol×(7-2)=0.5mol,个数为0.5NA或3.01×1023,100mL12mol/L的浓盐酸中含有HCl的物质的量为0.1L×12mol/L=1.2mol,与KMnO4反应后溶液中剩余Cl-的物质的量为1.2mol-2×n(Cl2)=1.2mol-2×0.25mol=0.7mol,向反应后的溶液中加入足量的硝酸银,生成AgCl沉淀的质量为0.7mol×143.5g/mol=100.45g,故答案为:5.6;0.5NA(或3.01×1023);100.45;
(3). 标准状况下6.72L HCl的物质的量为6.72L÷22.4L/mol=0.3mol,溶于水形成250mL溶液,HCl的物质的量浓度为:c(HCl)=0.3mol÷0.25L=1.2mol/L,取出10mL于锥形瓶中,向锥形瓶中滴加0.5mol/LBa(OH)2溶液,二者反应的化学方程式为:Ba(OH)2+2HCl=BaCl2+2H2O,根据方程式可知,恰好反应时,消耗Ba(OH)2的物质的量为0.01L×1.2mol/L÷2=0.006mol,体积为0.006mol÷0.5mol/L=0.012L=12mL,故答案为:1.2;12。


 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】根据下图所给信息,得出的结论正确的是( ) 
A.碳的燃烧热为b kJ/mol
B.2C(s)+O2(g)═2CO(g)△H=﹣2(b﹣a) kJ/mol
C.2CO2(s)═2CO(g)+O2(g)△H=+a kJ/mol
D.C(s)+O2(g)═CO2(g)△H<﹣b kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 实验室应将钠保存在煤油中
B. 钠放置在空气中,会迅速被氧化而生成淡黄色的氧化钠
C. 将铝箔在酒精灯上加热,现象为铝箔融化但并不滴落是因为氧化铝的熔点高于铝单质
D. 金属钠失火不可用水来灭火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、L、M五种元素的原子序数依次增大.X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素.
回答下列问题:
(1)L的元素符号为;M在元素周期表中的位置为;五种元素的原子半径从大到小的顺序是(用元素符号表示).
(2)Z、X两元素按原子数目比l:3和2:4构成分子A和B,A的电子式为 , B的结构式为 .
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为 , 其最高价氧化物对应的水化物化学式为 . 该族2~5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1mol硒化氢反应热的是(填字母代号).
a.+99.7molL﹣1 b.+29.7molL﹣1 c.﹣20.6molL﹣1 d.﹣241.8kJmol﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D 4种元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.
(1)B元素的名称为;
(2)A,B形成的化合物的电子式为 .
(3)C的元素符号为 , C的最高价氧化物的化学式为 .
(4)D的最高价氧化物对应的水化物的化学式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)0.5 mol的Fe含_______个铁原子(用6.02×1023表示阿伏加德罗常数),质量是_____g;
(2)3mol CO2在标准状况下的体积为___________L,摩尔质量为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是( )
A.利用电池外壳的金属材料
B.防止电池中汞、镉和铅等重金属离子对土壤和水源造成污染
C.不使电池中渗透的电解液腐蚀其他物品
D.回收其中石墨电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种有机光电材料中间体.实验室由芳香化合物A制备H的一种合成路线如下: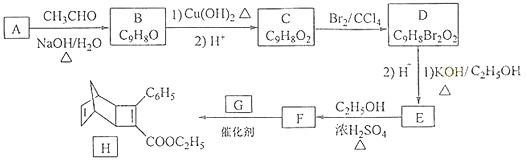
已知:①RCHO+CH3CHO ![]() RCH=CHCHO+H2O
RCH=CHCHO+H2O
② ![]() +
+ ![]()
![]()
![]()
回答下列问题:
(1)A的化学名称为为 .
(2)由C生成D和E生成F的反应类型分别为、 .
(3)E的结构简式为 .
(4)G为甲苯的同分异构体,由F生成H的化学方程式为 .
(5)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO2 , 其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:2:1:1,写出2种符合要求的X的结构简式 .
(6)写出用环戊烷和2﹣丁炔为原料制备化合物 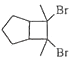 的合成路线(其他试剂任选).
的合成路线(其他试剂任选).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com