
| |||||||||||||||||||
科目:高中化学 来源:河北省冀州中学2010-2011学年高二下学期第三次月考化学试题 题型:058
(1)菠菜营养丰富,素有“蔬菜之王”之称,在营养价值上是一种高效的补铁剂.某化学小组欲设计实验方案,探究菠菜中是否存在铁元素与草酸及可溶性草酸盐.甲同学查阅资料得知:草酸又名乙二酸,化学式为H2C2O4,是一种二元有机弱酸,具有较强的还原性.甲同学依据上述信息推测,菠菜中铁元素呈________价,其理由是________.甲同学同时设计实验方案,验证其推测是否正确.请简述实验方案________.
(2)乙炔是有机合成工业的一种原料.工业上曾用![]() 与水反应生成乙炔.
与水反应生成乙炔.
①CaC2中![]() 与
与![]() 互为等电子体,
互为等电子体,![]() 的电子式可表示为________;1 mol
的电子式可表示为________;1 mol ![]() 中含有的
中含有的![]() 键数目为________.
键数目为________.
②乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N).丙烯腈分子中碳原子轨道杂化类型是________;分子中处于同一直线上的原子数目最多为________.
查看答案和解析>>
科目:高中化学 来源:昆山市2006-2007学年高二学业水平测试模拟试题 化学-苏教版 题型:058
| |||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源:天利38套《2008全国各省市高考模拟试题汇编(大纲版)》、化学 大纲版 题型:058
请回答(1)和(2)两小题:
(1)下列说法正确的是________(选填序号)
A.在进行物质检验时,一般先对试样进行外观观察,确定其状态、颜色、气味等
B.配制银氨溶液时,应把硝酸银溶液逐滴加入氨水中
C.一般在实验室点燃可燃性气体时,必须先要检验纯度
D.测定硫酸铜晶体结晶水的质量分数时,若用潮湿的坩埚会使测定结果偏小
E.酸碱中和滴定实验中根据碱式滴定管的两次读数得出NaOH溶液体积为22.0 mL
F.实验室制取氯气等有毒气体时,必须在密闭体系或通风橱中进行
(2)补铁剂中铁元素的含量是质检部门衡量其质量的重要指标,实验主要包括如下步骤:
①配制0.01 mol/L到0.008 mol/L等一系列浓度的[Fe(SCN)6]3-(红色)溶液作为标准比色液
②样品处理:

③准确量取一定体积的待测液于比色管中,加入稍过量的KSCN溶液,并稀释到10 mL.
④比色:选取与待测液颜色一致或相近的标准比色液即可判断待测液的浓度.
试回答下列问题:
①配制100 mL 0.01 mol/L标准溶液,需要的玻璃仪器有:烧杯、玻璃棒、量筒,还需要:________、________.
②步骤②脱色过程包括加入:________(填:脱有机色素的吸附剂名称)→搅拌煮沸→冷却→________(填操作).
③步骤②样品处理中,氧化的目的是________.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
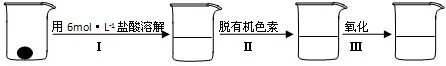
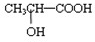 与铁粉作用生成的,请写出上述步骤②反应Ⅰ的化学方程式:______.
与铁粉作用生成的,请写出上述步骤②反应Ⅰ的化学方程式:______.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com