
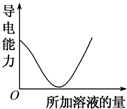
 如图所示,纵坐标表示导电能力,横坐标表示所加溶液的量,以下各组反应,符合该图的是( )
如图所示,纵坐标表示导电能力,横坐标表示所加溶液的量,以下各组反应,符合该图的是( )| A. | 氨水中滴加与其浓度相同的盐酸 | |
| B. | NaOH溶液中滴加与其浓度相同的稀盐酸 | |
| C. | CH3COOH溶液中滴加与其浓度相同的KOH溶液 | |
| D. | Ba(OH)2溶液中滴加与其浓度相同的H2SO4溶液 |
分析 溶液导电能力与离子浓度成正比,与电荷成正比,与电解质强弱无关;根据图知,溶液导电能力先减小后增大,说明溶液中离子浓度先减小后增大,据此分析解答.
解答 解:A.一水合氨是弱电解质,氨水中离子浓度较小,加入稀盐酸后,二者反应生成强电解质氯化铵,离子浓度增大,所以溶液导电能力先增大,故A错误;
B.NaOH、HCl都是强电解质,二者反应生成强电解质NaCl,离子浓度变化不大,所以溶液导电能力变化不大,故B错误;
C.醋酸是弱电解质,溶液中离子浓度较小,加入相同浓度的KOH溶液,二者反应生成强电解质醋酸钾,离子浓度变化不大,则溶液导电能力变化不大,故C错误;
D.氢氧化钡和稀硫酸反应生成难溶性硫酸钡和弱电解质水,导致溶液中离子浓度减小,溶液导电能力减小,当二者恰好反应时,溶液中只有水,离子浓度很小,溶液导电能力接近于0,继续滴加稀硫酸,溶液中离子浓度增大,溶液导电性增强,故D正确;
故选D.
点评 本题考查图象分析,为高频考点,明确离子浓度与溶液导电性强弱关系是解本题关键,溶液导电性与电解质强弱无关,为易错点.


科目:高中化学 来源: 题型:多选题
| A. | P的平均反应速率是0.15mol/(L•min) | B. | Q的转化率是25% | ||
| C. | Q的平衡浓度是1mol/L | D. | x的值为2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑦ | B. | ③⑤⑧ | C. | ④⑥ | D. | ②③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:2:2:4 | B. | 1:1:1:1 | C. | 2:1:1:2 | D. | 1:2:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一氯甲烷(CH3Cl) | B. | 甲基(-CH3 ) | C. | 碳负离子(CH3-) | D. | 乙烯(C2H4) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | R可能位于VA族 | B. | R的氢化物的水溶液一定属于强酸 | ||
| C. | RO3-中的R只能被还原 | D. | R的氢化物的水溶液可能显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.6mol•L-1•S-1 | B. | 0.8mol•L-1•S-1 | C. | 0.4mol•L-1•S-1 | D. | 2.4mol•L-1•S-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com