
【题目】SO2催化氧化过程中,不符合工业生产实际的是
A. 采用热交换器循环利用能量 B. 压强控制为20~50MPa
C. 反应温度控制在450℃左右 D. 使用V2O5作催化剂
科目:高中化学 来源: 题型:
【题目】自热食品已成为现代生活的时尚。自热食品包装中有两包发热剂,在这两包发热剂中最适合盛饭的物质是( )
A. 熟石灰和水 B. 生石灰和水 C. 氯化钠和水 D. 氯化铵和氢氧化钡晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氨的水溶液显弱碱性,其原因为___________________(用离子方程式表示), 0.1 molL-1的氨水中加入少量的NH4Cl固体,溶液的pH________(填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度__________(填“增大”或“减小”);
(2)25℃,两种酸的电离平衡常数如下表。
Ka1 | Ka2 | |
H2SO3 | 1.3×10-2 | 6.3×10-8 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
①HSO3-的电离平衡常数表达式K=___________________;
②0.10molL-1Na2SO3溶液中离子浓度由大到小的顺序为___________________;
③H2SO3溶液和NaHCO3溶液反应的离子方程式为___________________;
(3)银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电池和照明器材等领域亦有广泛应用。已知Ksp(AgCl)=1.8×10-10,若向5mL0.018molL-1的AgNO3溶液中加入5mL0.020molL-1的盐酸,混合后溶液中的Ag+的浓度为______molL-1,pH为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 铜片插入到硝酸银溶液中 Cu + Ag+![]() Cu2+ + Ag
Cu2+ + Ag
B. 硫酸镁跟氢氧化钡反应 Ba2++SO42-![]() BaSO4↓
BaSO4↓
C. 三氯化铁溶液与氢氧化钠溶液反应: FeCl3+3OH-![]() Fe(OH)3↓+3Cl-
Fe(OH)3↓+3Cl-
D. 氢氧化钠溶液和硫酸溶液反应 H++OH-![]() H2O
H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向密闭容器中充入物质A和B,发生反应aA(g)+bB(g)![]() cC(g)。反应过程中,物质A的体积分数
cC(g)。反应过程中,物质A的体积分数
和C的体积分数随温度(T)的变化曲线如图所示。下列说法正确的是
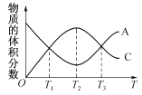
A.该反应在T1、T3温度时达到化学平衡 B.该反应在T2温度时达到化学平衡
C.该反应的逆反应是放热反应 D.升高温度,平衡会向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 标准状况下,22.4L水中所含的分子数约为6. 02×1023个。
B. 1 mol Cl2中含有的原子数为NA
C. 标准状况下,4.48L氧气和氮气的混合物含有的分子数约为1.204×1023个。
D. 从1L 0.5 mol/L NaCl溶液中取出100ml,剩余溶液中NaCl的物质的量浓度为0.45 mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于取代反应的是
A. 乙烯通入酸性高锰酸钾溶液中
B. 苯与液溴混合后撒入铁粉
C. 在镍做催化剂的条件下,苯与氢气反应
D. 乙烯通入溴水中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com