
| 试剂 | |
| 乙烷混有少量乙烯 | |
| 溴苯混有少量溴单质 |
 .
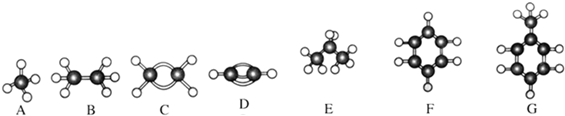
. 分析 I.根据球棍模型可知,A为CH4,B为CH3CH3,C为CH2=CH2,D为CH≡CH,E为CH3CH2CH3,F为苯,G为甲苯,
(1)常温下,分子中含有碳原子个数不大于4的烃为气态烃,根据其球棍模型判断,分子中含有碳氢原子个数比最大即为含碳量最高的.
(2)根据烃的球棍模型确定一卤代烃的同分异构体种类;
(3)实验室用碳化钙和水反应制取乙炔;
(4)苯和溴在催化剂、加热条件下生成溴苯;
II.乙烯与溴水反应,而乙烷不能;
溴与NaOH反应后,与溴苯分层;
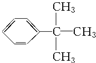
Ⅲ.C10H14的一烷基取代苯,则除苯环外只有1个侧链,侧链为丁烷烷基的碳链同分异构体有: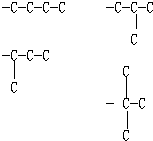 ,以此来解答.
,以此来解答.
解答 解:I.根据图示结构可知:A为甲烷,B为乙烷,C为乙烯,D为乙炔,E为丙烷,F为苯,G为甲苯,
(1)常温下,分子中含有碳原子个数不大于4的烃为气态烃,根据其球棍模型判断,分子中含有碳氢原子个数比最大即为含碳量最高的,所以含碳量最大的是乙炔.
故答案为:D;
(2)甲烷、乙烷、乙烯、乙炔、苯的一卤代物都只有1种,丙烷的一卤代物有2种,甲苯的有一卤代物有4种,故答案为:G;
(3)实验室用碳化钙和水反应制取乙炔,反应方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑,故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑;
(4)F为苯,可与溴发生取代反应,反应的方程式为C6H6+Br2$\stackrel{FeBr_{3}}{→}$C6H5Br+HBr,故答案为:C6H6+Br2$\stackrel{FeBr_{3}}{→}$C6H5Br+HBr;
II.II.乙烯与溴水反应,而乙烷不能,则除杂试剂为溴水;
溴与NaOH反应后,与溴苯分层,则除杂试剂为NaOH溶液,
故答案为:
| 试剂 | |
| 乙烷混有少量乙烯 | 溴水 |
| 溴苯混有少量溴单质 | NaOH溶液 |
 ,其中一种为
,其中一种为 ,
, .
.点评 本题考查有机物的结构与性质及混合物分离提纯,为高频考点,把握有机物的组成、性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意同分异构体为解答的难点,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 氨和联氨(N2H4)是氮的两种常见化合物,在工农业生产中有重要的应用.
氨和联氨(N2H4)是氮的两种常见化合物,在工农业生产中有重要的应用. [N2H5•H2O]++H+.下列盐酸肼溶液中的离子浓度关系正确的是ac(填序号).
[N2H5•H2O]++H+.下列盐酸肼溶液中的离子浓度关系正确的是ac(填序号).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中滴入盐酸,有无色无味的气体产生,说明某溶液一定含有含CO32- | |
| B. | 向某溶液中加入NaOH溶液,并加热,产生的气体能使湿润的红色石蕊试纸变蓝,说明某溶液中一定含有NH4+ | |
| C. | 向某溶液中滴加氯化钡溶液,得到白色沉淀,说明某溶液中一定含有SO42- | |
| D. | 向某溶液中加入过量的NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明某溶液中一定含有Fe2+,一定不含有Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Na+)>c(CH3COO-)的CH3COOH与CH3COONa的混合溶液 | |
| B. | 常温下,pH=3的CH3COOH与pH=11的NaOH溶液等体积混合 | |
| C. | 含OH-的溶液 | |
| D. | 滴加甲基橙后溶液显红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 :2-甲基-1,3-丁二烯;该物质与溴单质以物质的量之比1:1发生加成反应可能的产物有3 种;
:2-甲基-1,3-丁二烯;该物质与溴单质以物质的量之比1:1发生加成反应可能的产物有3 种; :苯甲醛;
:苯甲醛;查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 其一氯代物只有一种 | B. | 其二氯代物有三种同分异构体 | ||
| C. | 常温下为气体 | D. | 它与苯乙烯(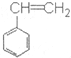 )互为同分异构体 )互为同分异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com