
【题目】氨法溶浸氧化锌烟灰制取高纯锌的工艺流程如下图所示。溶浸后氧化锌烟灰中锌、铜、镉、砷元素分别以Zn(NH3)42+、Cu(NH3) 42+、Cd(NH3)42+、AsCl52-的形式存在。
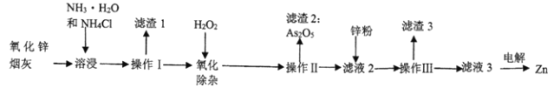
请回答下列问题:
(1)当NH4Cl、NH3·.H2O的混合溶液中存在c(NH4+)=c(Cl-)时,溶液呈___(填“酸”、“碱”或“中”)性。
(2)Zn(NH3)42+中Zn的化合价为____,“溶浸”中ZnO发生反应的离子方程式为____。
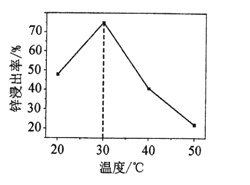
(3)一定时间内,锌浸出率与温度的关系如图所示,分析30℃时锌浸出率最高的原因为_____。
(4)实验室实现操作II”所用的玻璃仪器有___,玻璃棒和烧杯等 “滤渣3”的主要成分为__。
(5)“电解”时Zn(NH3)42+在阴极放电的电极反应式为_____。电解后的电解液经补充__(写一种物质的化学式)后可返回“溶浸”工序继续使用。
【答案】中性 +2 ZnO+2NH3H2O+2NH4+=Zn(NH3)42++3H2O 低于30℃时,浸出反应速度随温度的升高而增大;超过30℃,氨气逸出导致浸出反应速度下降 漏斗 Cu、Cd Zn(NH3)4 2++2e-=Zn+4NH3↑或Zn(NH3)42++2e -+4H2O=Zn+4NH3H2O NH3 (或NH3H2O)
【解析】
由流程可知,氧化锌烟灰加入氨水、氯化铵进行溶浸,溶浸后氧化锌烟灰中锌、铜、镉、砷元素分别以Zn(NH3)42+、Cu(NH3) 42+、Cd(NH3)42+、AsCl52-的形式存在,滤渣1为Pb,加入过氧化氢,AsCl52-转化为As2O5除去,过滤后加入锌粉还原,可除去Cu等,滤液主要含有Zn(NH3)42+,电解可生成高纯度锌,以此解答该题。
(1)在该溶液中存在电荷守恒:c(H+)+c(NH4+)=c(Cl-)+c(OH-),由于c(NH4+)=c(Cl-),所以c(H+)= c(OH-),因此溶液显中性;
(2)在Zn(NH3)42+中由于N为-3价,H为+1价,该离子带有2个单位的正电荷,所以Zn的化合价为+2价,氧化锌烟灰加入氨水、氯化铵进行溶浸, ZnO发生反应产生Zn(NH3)42+及H2O,发生反应的离子方程式为ZnO+2NH3H2O+2NH4+=Zn(NH3)42++3H2O。
(3)在低于30℃时,升高温度,化学反应速率加快,更多的ZnO反应产生Zn(NH3)42+,锌浸出率增大,但温度过高,氨水会分解,产生的氨气挥发逸出,导致反应速率降低,锌的浸出率降低;
(4)“氧化除杂”中,AsCl52-转化为As2O5除去,经过过滤将As2O5过滤除去,所以操作II使用的玻璃仪器有漏斗、玻璃棒和烧杯等;经过滤得到的滤液中含有Zn(NH3)42+、Cu(NH3) 42+、Cd(NH3)42+,向其中加入Zn,反应后会反应产生Cu、Cd,所以“滤渣3”的主要成分为Cu、Cd;
(5)“电解”时Zn(NH3)42+在阴极放电,发生还原反应生成锌,电极反应式为Zn(NH3)42++2e-=Zn+4NH3,也可以写为Zn(NH3)42++2e -+4H2O=Zn+4NH3H2O;反应产生的NH3或NH3H2O可以再用于溶解氧化锌烟灰,因此可以循环利用的物质是NH3 (或NH3H2O)。


科目:高中化学 来源: 题型:
【题目】短周期主族元素A、B、C、D、E的原子序数依次增大,其中A、D同主族,B、C、D、E同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径最大的主族元素,C原子的质子数比B原子的质子数多2个。请回答下列问题:
(1)B元素的名称为___________,E的元素符号为___________
(2)A、B两种元素可形成化学式为B2A、B2A2等化合物,则B2A2的电子式为_____。
(3)将B2A2投入到B2D的水溶液中可生成D的单质,发生反应的离子方程式为:______________________
(4)DA2与E元素的单质在水中反应的离子方程式为:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最新科技报道,美国夏威夷联合天文中心的科学家发现了新型氢粒子,这种新粒子是由3个氢原子核(只含质子)和2个电子构成的。对于这种粒子,下列说法中正确的是
A.是氢的一种新的同素异形体B.它比一个普通H2分子多一个氢原子核
C.是氢的一种新的同位素D.它的组成可用H3表示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把0.4molX气体和0.6molY气体混合于2L密闭容器中,使它们发生如下反应:4X(g)+5Y(g) ![]() nZ(g)+6W(g)。2min末已生成0.3molW,若测知以Z的浓度变化表示的反应速率为0.05mol/(L·min),试计算
nZ(g)+6W(g)。2min末已生成0.3molW,若测知以Z的浓度变化表示的反应速率为0.05mol/(L·min),试计算
(1)前2min内用W的浓度变化表示的平均反应速率为_______________。
(2)2min末时Y的浓度为_____________________________。
(3)化学反应方程式中n=_____________________________。
(4)2min末,恢复到反应前温度,体系内压强是反应前压强的__________倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1mol H2燃烧生成液态水时放出285.8kJ 热量,下列表示该反应的热化学方程式正确的是
A. 2H2(g)+O2(g)=2H2O(l) △H =-142.9kJ/mol
B. 2H2(g)+O2(g)=2H2O(l) △H =+571.6 kJ/mol
C. 2H2(g)+O2(g)=2H2O(l) △H =-57l.6 kJ/mol
D. 2H2+O2=2H2O △H =-571.6kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是对10mL一定物质的量浓度的盐酸用一定物质的量浓度的NaOH溶液滴定的图像,依据图像推出盐酸和NaOH溶液的物质的量浓度是下表内各组中的
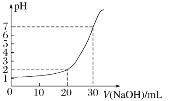
选项 溶液 | A | B | C | D |
C(HCl)/mol·L-1 | 0.12 | 0.04 | 0.03 | 0.09 |
c(NaOH)/mol·L- | 0.04 | 0.12 | 0.09 | 0.03 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图中装置进行实验,实验一段时间后,现象与预测不一致的是
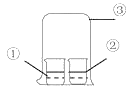
①中物质 | ②中物质 | 实验预测 | |
A | 浓氨水 | 酚酞试液 | ②中溶液变为红色 |
B | 浓硝酸 | 淀粉KI溶液 | ②中溶液变为蓝色 |
C | 浓盐酸 | 浓氨水 | 大烧杯中有白烟 |
D | 饱和的亚硫酸溶液 | 稀溴水 | ②中无明显变化 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应伴随能量变化,其中能量的主要形式是热能。
I:如图所示,把试管放入盛有25℃饱和澄清石灰水的烧杯中,往试管中放入几小块镁片,再用滴管滴入5mL盐酸于试管中,试回答下列问题:
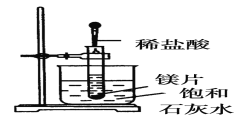
(1)实验中观察到的现象是________________________。
(2)产生上述现象的原因是________________________。
(3)写出有关反应的离子方程式__________________________。
(4)由实验推知,MgCl2和H2的总能量________(填“大于”“小于”或“等于”)镁片和HCl的总能量。
II:从能量变化的角度研究反应:2H2+O2=2H2O。
(1)如图能正确表示该反应中能量变化的是_________。
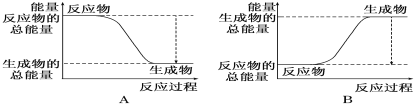
(2)已知断开或形成1 mol化学键吸收或放出的能量,叫做该化学键的键能,单位为kJ·mol-1。一些键能数据如下表:
化学键 | H—H | O=O | H—O |
键能(kJ·mol-1) | 436 | 496 | 463 |
请回答:
断裂反应物2 mol H2和1 mol O2的化学键,需要_______的总能量为______kJ;形成生成物2 mol H2 O的化学键,需要______的总能量为______kJ。所以该反应能量变化值的大小 ____________ kJ(填数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物A分子由C、H、O三种元素组成,其相对分子质量为120,0.1molA在足量的氧气中充分燃烧后生成0.8mol CO2 和7.2g H2O;A可以发生银镜反应,其苯环上的一卤代物有三种。
(1)A的分子式是_________,A中含氧官能团的名称是________________,A的结构简式是_______________。
已知:I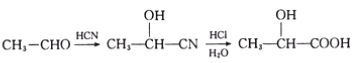
II.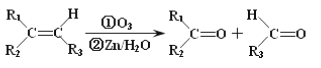
现有如下转化关系:
![]()
其中D能使溴的四氯化碳溶液褪色,F继续被氧化生成G,G的相对分子质量为90。
(2)C可能具有的化学性质是____________。(请填字母)
① 能与H2发生加成反应;② 能在碱性溶液中发生水解反应;③ 能与甲酸发生酯化反应;④ 能与Ag(NH3) 2OH溶液发生银镜反应;⑤能与氢氧化钠溶液反应
A.①②③ B.①③⑤ C.①②③⑤ D.②③④⑤
(3)① 写出C→D的化学反应方程式是________________________________________;反应类型是____________。
②在催化剂条件下,C生成高聚物的化学方程式是_________________________________。
(4)请写出化合物C可能的同分异构体结构简式是___________________________。须同时符合下列条件:
①属于酯类化合物;
②遇三氯化铁溶液显紫色;
③与新制氢氧化铜悬浊液共热可生成红色沉淀;
④苯环上的一卤代物只有一种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com