
| A. | 锌粒与稀硫酸的反应 | |
| B. | 灼热的木炭与CO2反应 | |
| C. | 碳酸钙高温下分解 | |
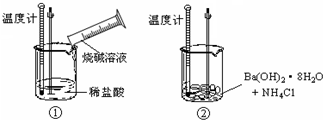
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
分析 存在元素的化合价变化的反应为氧化还原反应,常见的吸热反应有:Ba(OH)2•8H2O与NH4Cl反应、大多数的分解反应、C(或氢气)参加的氧化还原反应等,以此来解答.
解答 解:A、锌粒与稀硫酸的反应为放热反应,Zn、H元素的化合价变化,属于氧化还原反应,故A不选;
B、灼热的木炭与CO2反应为吸热反应,且C元素的化合价变化,属于氧化还原反应,故B选;
C、碳酸钙高温下分解为吸热反应,但没有元素的化合价变化,不属于氧化还原反应,故C不选;
D、Ba(OH)2•8H2O与NH4Cl反应为吸热反应,但没有元素的化合价变化,不属于氧化还原反应,故D不选,
故选B.
点评 本题考查氧化还原反应,为高考高频考点,侧重反应类型判断的考查,注意化合价角度及归纳常见的吸热反应分析,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该化合物可能为2甲基2丙醇 | B. | 该化合物为2丁醇的同分异构体 | ||
| C. | 该化合物可能为乙醚 | D. | 该化合物为乙醚的同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 配制950ml 2.3mol/LH2SO4溶液需要取该硫酸125.0mL | |
| B. | 1molAl与足量该硫酸反应产生3g氢气 | |
| C. | 该硫酸在空气中露置,溶质的质量分数会逐渐减小 | |
| D. | 该硫酸不能用来干燥二氧化硫 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2L氧气含有的原子数目为NA | |
| B. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA | |
| C. | 在标准状况下,22.4 L水的质量约为18g | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com