
10克Fe2O3、SiO2、Al2O3混合物加入足量的100mL x mol/L稀硫酸中,过滤,然后加入10mol/L NaOH溶液,产生沉淀的质量和加入NaOH溶液体积如右图.以下叙述错误的是()

A. 滤出的物质为SiO2 B. 可求出x的值
C. 可求出Al2O3的质量分数 D. 可求出Fe2O3的质量分数
考点: 有关混合物反应的计算.
专题: 计算题.
分析: Fe2O3、SiO2、Al2O3混合物加入足量的硫酸中,过滤所得沉淀为SiO2,当加入NaOH100mL时沉淀为氢氧化铁和氢氧化铝,溶液溶质为硫酸钠,加入NaOH110mL时,氢氧化铝全部溶解,可计算氧化铝的质量,由于滤液中过量的酸的量和沉淀的总质量未知,则不能确定氧化铁的质量,以此解答该题.
解答: 解:A.二氧化硅与硫酸不反应,则滤出的物质为SiO2,故A正确;
B.当加入NaOH100mL时沉淀为氢氧化铁和氢氧化铝,溶液溶质为硫酸钠,根据H2SO4﹣Na2SO4﹣2NaOH可知n(Na)=2n(硫酸),可知x的值,故B正确;
C.加入NaOH110mL时,氢氧化铝全部溶解,则根据Al(OH)3+NaOH=NaAlO2+2H2O可知Al2O3的质量分数,故C正确;
D.由于滤液中过量的酸的量和沉淀的总质量未知,则不能确定氧化铁的质量,故D错误.
故选D.
点评: 本题考查混合物的计算,注意根据图象判断各反应,根据反应方程式计算该题,题目难度不大.


科目:高中化学 来源: 题型:
在给定条件下,下列划横线的物质在化学反应中能被完全消耗的是()
A. 标准状况下,将1 g铝片投入20 mL 18.4 mol•L﹣1的硫酸中
B. 向100 mL 3 moI•L﹣1的硝酸中加入5.6 g铁
C. 用50 mL 18 mol•L﹣1浓硫酸与足量Cu共热(指其中的硫酸被完全消耗)
D. 在5×107 Pa、500℃和铁触媒催化的条件下,用3 mol氢气和2 mol氮气合成氨
查看答案和解析>>
科目:高中化学 来源: 题型:
以下有关物质的质量分数和物质的量浓度的叙述正确的是()
A. 等体积硫酸铁、硫酸铜、硫酸钾溶液分别与足量的氯化钡溶液反应,若生成硫酸钡沉淀的质量相等,则三种硫酸盐溶液的物质的量浓度之比为1:1:1
B. Na2O2和Na2O各0.1mol分别放入100g水中,所得溶液的物质的量浓度不相等
C. 质量分数分别为5%和15%的氨水等体积混合后所得溶液的质量分数为10%
D. 20℃时,饱和KCl溶液的密度为1.174g•cm﹣3,物质的量浓度为4.0 mol•L﹣1,则此溶液中KCl的质量分数为 ×100%
×100%
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)有以下八种饱和溶液:①Ba(NO3)2;②Ca(OH)2;③Ca(ClO)2;④CaCl2;
⑤Na2CO3;⑥NaAlO2;⑦NH3和NaCl;⑧Na2SiO3.向其中分别持续通入CO2,最终能得到沉淀或析出晶体的是 (请填序号)
(2)氯化铵水溶液显酸性,请用离子方程式表示原因 ;
如往氯化铵浓溶液中加入镁粉,反应剧烈且放出气体能使湿润红色石蕊试纸变蓝色,请写出相应离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A. 淀粉、纤维素和油脂都属于天然高分子化合物
B. 合成纤维、人造纤维及碳纤维都属于有机高分子材料
C. 蔗糖、淀粉、油脂及其水解产物均为非电解质
D. 石油是混合物,其分馏产品汽油也为混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
某探究小组在实验室中用铝土矿(主要成分为Al2O3,还含有Fe2O3、SiO2)提取氧化铝.回答下列问题:
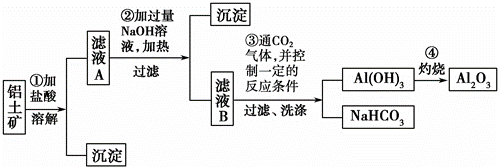
(1)在实验中需用1mol•L﹣1的NaOH溶液480mL,配制该溶液已有下列仪器:托盘天平(砝码)、胶头滴管、药匙、玻璃棒,还缺少的仪器 .在灼烧操作中用到下列仪器中的一种,其名称是 .
写出步骤①中发生反应的离子方程式 .
(3)操作③中的洗涤操作如何进行? .
(4)甲同学在实验室中用如图装置制备CO2气体,并通入滤液B中制备Al(OH)3时,结果没有产生预期现象.
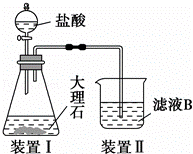
乙同学分析认为:甲同学通入CO2的量不足是导致实验失败的原因之一,你认为乙的分析是否合理? .若合理,请用离子方程式解释其原因 (若你认为不合理,该空不作答).
丙同学分析认为:甲同学通入的CO2中含有HCl气体,也是导致实验失败的原因,在实验中增加某装置可解决这个问题.请帮助丙同学画出该装置图,并注明试剂名称.
查看答案和解析>>
科目:高中化学 来源: 题型:
向体积为2L的固定密闭容器中通入3mol X气体,在一定温度下发生如下反应:2X(g)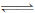 Y(g)+3Z(g)
Y(g)+3Z(g)
(1)经5 min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的速率为__________mol • L﹣1 • min﹣1。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为甲:v(X)=3.5 mol • L﹣1 • min﹣1;乙:v(Y)=2 mol • L﹣1 • min﹣1;丙:v(Z)= 4.5mol • L﹣1 • min﹣1;丁:v (X)= 0.075 mol • L﹣1 • s﹣1。若其他条件相同,温度不同,则温度由高到低的顺序是(填序号)______________________。
(3)若向达到(1)的平衡体系中充入氮气,则平衡___________(填“向左”“向右”或“不”)移动;若从达到(1)的平衡体系中移走部分Y气体,则平衡___________(填“向左”“向右”或“不”)移动。
(4)若在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体,则平衡后X的转化率与(1)的平衡中X的转化率相比较
A.无法确定
B.前者一定大于后者
C.前者一定等于后者
D.前者一定小于后者
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol,达到平衡时仍与(1)的平衡等效,则:a、b、c应该满足的关系为__________________。
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol,达到平衡时仍与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,则c的取值范围应该为______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com