
【题目】下列关于物质“反应程度”的说法正确的是( )
A.一定条件下,2molSO2与足量O2反应可得到2molSO3
B.含4mol HCl的浓盐酸与足量的MnO2加热反应可制备1mol Cl2
C.10mL 18.0mol/L H2SO4与足量铜加热反应可制备0.09molSO2
D.一定条件下,1mol N2与3mol H2反应可制备1.0mol NH3
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】已知: X(g)+2Y(g) ![]() 3Z(g) ΔH=-a kJ·molˉ1(a>0)。下列说法正确的是
3Z(g) ΔH=-a kJ·molˉ1(a>0)。下列说法正确的是
A. 达到化学平衡状态时,Y 的正反应速率和 Z 的逆反应速率相等
B. 达到化学平衡状态时,X、Y、Z 的浓度之比为 1 : 2 : 3
C. 达到化学平衡状态时,反应放出的总热量一定小于 a kJ
D. 0.2 mol X 和 0.2 mol Y 充分反应生成 Z 的物质的量一定小于 0.3 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铁屑为原料制备三草酸合铁(Ⅲ)酸钾(K3[Fe(C2O4)3])的化学方程式依次为:
①Fe(s)+H2SO4=FeSO4+H2↑
②FeSO4+H2C2O4+2H2O = FeC2O4·2H2O↓+H2SO4
③2FeC2O4·2H2O+H2O2+H2C2O4+3K2C2O4=2K3[Fe(C2O4)3]+6H2O
已知: K3[Fe(C2O4)3]·3H2O 易溶于水, 难溶于乙醇。
回答下列问题:
(1)在反应①得到的 FeSO4溶液中, 需加入少量 H2SO4酸化, 目的是_________。
(2)为从反应③后的溶液得到 K3[Fe(C2O4)3]晶体, 某同学设计的实验步骤为: “加热蒸发—冷却结晶 —抽滤—洗涤 —干燥 ”,请评价该方案的合理性,并说明理由____________。
(3)为从反应③后的溶液中得到 K3[Fe(C2O4)3]·3H2O 晶体,请再设计另外一种实验方案(不要求写具体的实验操作)_______________。
(4)过滤K3[Fe(C2O4)3]·3H2O晶体有关的操作正确的是_______。
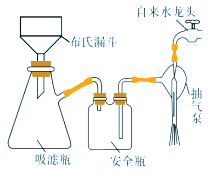
A.选择比布氏漏斗内径略小又能将全部小孔盖住的滤纸
B.放入滤纸后,直接用倾析法转移溶液和沉淀,再打开水龙头抽滤
C.洗涤晶体时,先关闭水龙头,用蒸馏水缓慢淋洗,再打开水龙头抽滤
D.抽滤完毕时,应先断开抽气泵和吸滤瓶之间的橡皮管,以防倒吸
(5)称取 5.00g 制得的晶体加水溶解,配成 250mL 溶液,取 25.00mL 于锥形瓶中,用0.100mol·L-1 酸性高锰酸钾标准溶液滴定,重复三次实验,平均消耗 12.00mL。 计算所得的样品中K3[Fe(C2O4)3]·3H2O的纯度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图。若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是
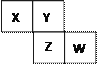
A. X的最常见气态氢化物的水溶液显碱性
B. 最高价氧化物对应水化物的酸性W比Z强
C. Z的单质与氢气反应比Y单质与氢气反应剧烈
D. X的原子半径小于Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室做钠和水反应的实验时,下列关于实验现象的描述错误的是
A.钠浮在水面上四处游动B.钠溶成小球,并且伴有“嘶嘶”声音
C.向反应后的溶液中加入酚酞,溶液颜色变红D.反应中有大量白色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碲(Te)及其化合物有许多优良性能,被广泛用于冶金、化工等领域。
(1)碲(Te)在周期表中的位置为________________________。碲化氢的还原性比H2S的还原性__________(填“强”或“弱”)。
(2)已知25℃时,亚碲酸(H2TeO3)的电离平衡常数:Ka1=1×10—3,Ka2=2×10—8。
①0.1mol/L H2TeO3溶液中H2TeO3的电离度约为__________;
②已知NaHTeO3的水溶液呈酸性,溶液中所有离子浓度大小顺序为____________________。
(3)TeO2微溶于水,易溶于较浓的强酸和强碱。工业上常用铜阳极泥(主要含Cu2Te,还含少量Ag、Au)为原料制备单质碲,其工艺流程如图:
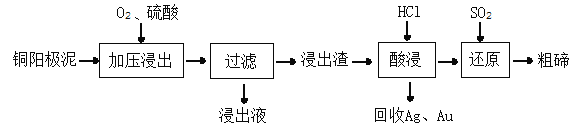
①已知浸出渣的主要成分是TeO2。写出“加压浸出”过程中的离子方程式________________________,该过程中,应控制溶液的pH为4.5~5.0,酸性不能太强的原因是__________________________。
②“酸浸”后将SO2通入浸出液即可制得单质碲,写出生成单质碲的化学方程式______________________。
③工业上还可以将铜阳极泥煅烧生成TeO2,然后碱浸,过滤,再对滤液进行电解的方法得到单质碲。已知电解时的电极均为石墨,则阴极的电极反应式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用12 mol·L-1的浓盐酸配制0.10 mol·L-1的稀盐酸500 mL。可供选择的仪器有:①玻璃棒、②烧瓶、③烧杯、④胶头滴管、⑤量筒、⑥500 mL容量瓶
回答下列问题:
(1)计算量取浓盐酸的体积为____ mL
(2)配制过程中,一定用不到的仪器是________(填序号)
(3)将浓盐酸加入适量蒸馏水稀释后,全部转移到500 mL容量瓶中,转移过程中玻璃棒的作用是____。转移完毕,用少量蒸馏水洗涤仪器2~3次,并将洗涤液全部转移到容量瓶中。然后缓缓地把蒸馏水直接注入容量瓶,直到液面接近刻度线1-2cm处。改用______滴加蒸馏水,使溶液的凹液面的最低处与刻度线相切。振荡、摇匀后,装瓶、贴签。
(4)在配制过程中,其他操作都准确,下列操作对所配溶液浓度的影响(填“偏高”、“偏低”或“无影响”)
①定容时,加蒸馏水超过刻度线,又用胶头滴管吸出重新加水至刻度线_______
②转移前,容量瓶中含有少量蒸馏水_________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com