
| 102×9.8% |
| 1 |
| 10 |
| 5 |
| 102-16×2-10×1 |
| 12 |
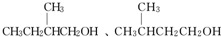 、(CH3)3CCH2OH,A、B形成酯的结构有4种,二者形成酯的结构为:CH3CH2CH2CH2COOCH2CH2CH2CH2CH3等,
、(CH3)3CCH2OH,A、B形成酯的结构有4种,二者形成酯的结构为:CH3CH2CH2CH2COOCH2CH2CH2CH2CH3等,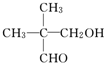 ,故答案为:
,故答案为: .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
A、ng该氯原子所含的电子数为
| ||
B、mg该氯原子的物质的量为
| ||
C、该氯原子的相对原子质量为
| ||
| D、0.5 mol该氯分子的质量为aNAg |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向20mL0.5mol/LFeBr2(aq)中通入224mLCl2(标准状况):2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
| B、在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入1~2滴盐酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O |
| C、酸性条件下,用FeCl3溶液吸收水煤气中的H2S,以回收硫元素、降低污染:2Fe3++H2S=2Fe2++S↓+2H+ |
| D、Ca(ClO)2浓溶液中通入足量的SO2:ClO-+SO2+H2O=2H++Cl-+SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 装置(气密性良好,试剂已添加) | 操作 | 现象 |
 |
打开分液漏斗活塞,逐滴加入浓氨水 | ⅰ.C中气体颜色变浅 ⅱ.稍后,C中出现白烟并逐渐增多 |


查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
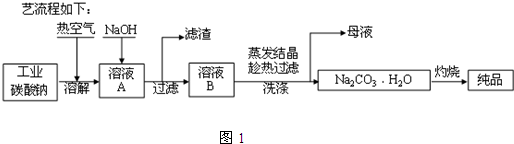
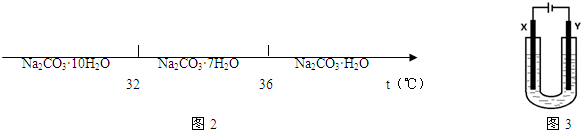
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7.8g Na2O2中离子总数为0.4NA |
| B、标准状况下,11.2L CCl4中的分子数为0.5NA |
| C、常温常压下,48g O2和O3的混合气体中含有的氧原子数为3NA |
| D、2.7g金属铝变为铝离子时失去的电子数为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com