
下列说法正确的是
A.能使pH试纸呈红色的溶液中可能大量存在以下离子:Na+、NH4+、I一、NO3-
B.将CH3COOH溶液和NaOH溶液等体积混合,该溶液中一定存在的关系式为:c(Na+)=c(CH3COO一)+c(CH3COOH)
C.pH=3的NaHA溶液中粒子浓度大小为:c( Na+)>c( HA一)>c(A2一)>c(H2A)>c(OH一)
D.CuSO4溶液遇到闪锌矿(ZnS)慢慢转化为铜蓝(CuS),是因为ZnS的溶解度大于CuS
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源:2014-2015河北省唐山市高二下学期开学调研化学试卷(解析版) 题型:选择题
下列溶液一定呈中性的是
A.c(H+)=c(OH-)=10-6 mol·L-1的溶液
B.pH=7的溶液
C.使石蕊试液呈紫色的溶液
D.酸与碱恰好完全反应生成正盐的溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市河东区高三一模理综化学试卷(解析版) 题型:选择题
化学与人类生产,生活密切相关。下列有关说法不正确的是
A.“海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化
B.福尔马林可浸制标本,利用了其使蛋白质变性的性质
C.医用酒精使用淀粉类植物发酵经蒸馏制成,浓度通常为75%
D.绚丽缤纷的烟花中添加了含钾,钙,钠,铜等金属元素化合物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省广安市高三二诊理综化学试卷(解析版) 题型:选择题
向甲、乙、丙三个密闭容器中充入一定量的X和Y,发生反应:x(g)+aY(g) 2Z(g)。各容器的反应温度、反应物起始量,反应过程中Z的浓度随时间变化关系分别以下图和下表表示。下列说法不正确的是
2Z(g)。各容器的反应温度、反应物起始量,反应过程中Z的浓度随时间变化关系分别以下图和下表表示。下列说法不正确的是
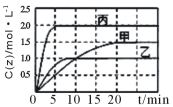
容器 | 甲 | 乙 | 丙 |
容积 | 0.5L | 0.5L | 1.0L |
温度/℃ | T1 | T2 | T2 |
反应物 起始量 | 1.0molX 0.5molY | 1.0molX 0.5molY | 4.0molX 2.0molY |
A.该反应温度升高,平衡常数减小
B.20min内甲容器中反应的平均速率: v(X) = 0.075mol·(L·min)-1
C.其他条件不变,若缩小乙的体积,Y的转化率不变
D.10min时,其他条件不变,向乙容器中再加入2 molZ,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省德阳市高三“二诊”考试化学试卷(解析版) 题型:推断题
(16分)从有机物A开始有如图所示的转化关系(部分产物略去)。 A在NaOH溶液中水解生成B、C和D,1mol F与足量的新制Cu(OH)2碱性悬浊液加热充分反应可生成2mol红色沉淀。分析并回答问题:
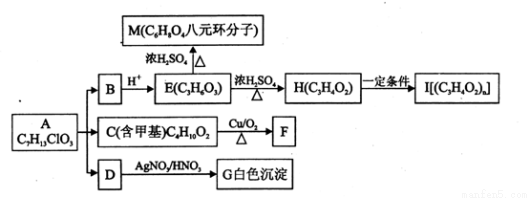
(1)A中含有的官能团有羟基、 (填写官能团名称)
(2)C的名称(系统命名)是 ;E—H的反应类型是 ;M的核磁共振氢谱有 组峰。
(3)C→F的化学方程式是 。
(4)F与足量新制Cu(OH)2反应的化学方程式是 。
(5)所有满足上述转化关系的A的结构简式是 。
(6)E的某同系物甲(C4H8O3)有多种同分异构体,其中含有酯基和羟基,且水解产物不存在两个羟基连在同一个碳上的同分异构体有 种。(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济宁市高三第一次模拟考试理综化学试卷(解析版) 题型:推断题
选做(12分)【化学一有机化学基础】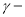 聚谷氨酸(
聚谷氨酸( )是一种具有水溶性、可生物降解、可食用的对人体和环境无毒的高分子聚合物,广泛应用于食品和医药等领域。下图是根据实际需要和目的,对
)是一种具有水溶性、可生物降解、可食用的对人体和环境无毒的高分子聚合物,广泛应用于食品和医药等领域。下图是根据实际需要和目的,对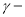 聚谷氨酸
聚谷氨酸 中的羧基进行化学修饰的路线,其中B、C、F均为高分子化合物。
中的羧基进行化学修饰的路线,其中B、C、F均为高分子化合物。

请回答:
(1)C的单体的结构简式为__________。D→E的反应类型是_________。
(2)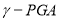 与NaHCO3溶液反应,可观察到的实验现象是_________。
与NaHCO3溶液反应,可观察到的实验现象是_________。
(3)下列关于CH3CH=CH2的说法中,正确的是__________(填字母序号)。
a.能使KMnO4酸性溶液褪色
b.它的同分异构体环丙烷属于不饱和烃
c.与HBr发生加成反应可得到两种产物
d.可以用溴的四氯化碳溶液鉴别丙烯和丙炔
(4)D的核磁共振氢谱有4个吸收峰,D发生银镜反应的化学方程式为:______________________。
(5)E与邻苯二甲酸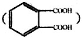 反应生成的产物DBP(C16H22O4)是广泛使用的增塑剂之一。DBP有多种同分异构体,其中符合下列条件的DBP的结构简式_____________________
反应生成的产物DBP(C16H22O4)是广泛使用的增塑剂之一。DBP有多种同分异构体,其中符合下列条件的DBP的结构简式_____________________
a.1mol化合物能与2molNaHCO3反应
b.苯环上只有两个相同的无支链取代基
c.苯环上的一氯取代物有三种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济宁市高三第一次模拟考试理综化学试卷(解析版) 题型:选择题
下列说法中不正确的是
A.8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) △H<O,则该反应能自发进行
B.pH相等的四种溶液:a.CH3COONa b.Na2CO3 c.NaHCO3 d.NaOH,则四种溶液中溶质的物质的量浓度由小到大顺序为:d<b<c<a
C.pH=2的一元酸和pH=12的二元强碱等体积混合:c(OH-)≤c(H+)
D.pH=9的CH3COONa溶液和pH=9的NH3·H2O溶液中水的电离程度相同
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省湖州市高三上学期期末考试化学试卷(解析版) 题型:实验题
(12分)某校化学小组的同学开展测定Na2SO3和NaCl的固体混合物中Na2SO3质量分数的探究实验,他们提出下列实验方案:
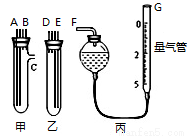
(1)小明同学用图中的发生、收集装置。甲、乙两试管各有两根导管,连接对应接口后,倒置盛稀硫酸的试管,发生反应,放出气体。则稀硫酸应置于 中(填“甲”或“乙”);G管可以用化学实验室里的一种常用仪器代替,你认为这种仪器的名称是 。仪器甲、乙接口的连接方式如下:A连接 ,C连接F;(填写接口的编号)
(2)小李同学用沉淀法测定Na2SO3的质量分数。
操作流程:
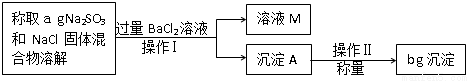
①操作Ⅱ的名称是 。
②操作Ⅰ之前,为判断所加BaCl2溶液是否过量, 设计如下方案,其中最合理的是 。
A.取少量上层清液,继续滴加稀H2SO4,若沉淀产生则说明BaCl2已过量。
B.待浊液澄清后,继续滴加BaCl2,若无沉淀产生则说明BaCl2已过量。
C.待浊液澄清后,继续滴加稀H2SO4,若沉淀产生则说明BaCl2已过量。
③根据以上数据得出Na2SO3的质量分数为 。
④小丽同学经认真分析,上述实验操作均正确,但发现实验结果与预期相差较大,请你推测可能的原因是 ,验证方法 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com