
【题目】化学学习小组进行如下实验。
Ⅰ.探究反应速率的影响因素
设计了如下的方案并记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20mol·L-1H2C2O4溶液、0.010mol·L-1KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
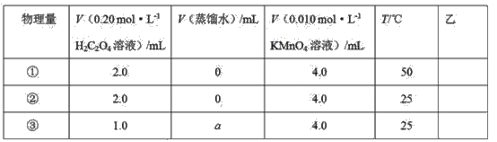
上述实验①、②是探究__对化学反应速率的影响;若上述实验②、③是探究浓度对化学反应速率的影响,则a为__;乙是实验需要测量的物理量,则表格中“乙”应填写__。
Ⅱ.测定H2C2O4·xH2O中x值
已知:M(H2C2O4)=90g·mol-1
①称取1.260g纯草酸晶体,将草酸制成100.00mL水溶液为待测液;
②取25.00mL待测液放入锥形瓶中,再加入适的稀H2SO4;
③用浓度为0.05000mol·L-1的KMnO4标准溶液进行滴定。
(1)请写出与滴定有关反应的离子方程式___。
(2)某学生的滴定方式(夹持部分略去)如下,最合理的是___(选填a、b)。
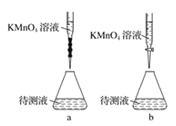
(3)由图可知消耗KMnO4溶液体积为___mL,滴定管内剩余的液体的体积为___。

A.20.9 B.大于20.9 C.小于29.1 D.大于29.1
(4)滴定过程中眼睛应注视___,滴定终点的现象为___。
(5)通过上述数据,求得x=___。以标准KMnO4溶液滴定样品溶液的浓度,未用标准KMnO4溶液润洗滴定管,引起实验结果___(偏大、偏小或没有影响)。
【答案】温度 1.0 溶液褪色时间/s 5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O b 20.00 D 锥形瓶中溶液颜色变化 当滴入最后一滴KMnO4标准溶液时,溶液由无色变为浅紫色,且半分钟内不恢复原来的颜色 2 偏小
【解析】
Ⅰ.实验①②是在相同浓度,不使用催化剂,不同温度下进行的实验探究;上述实验②③是探究浓度对化学反应速率的影响,则混合液的总体积必须相同;反应速率需要通过时间的快慢来体现;
Ⅱ.(1)H2C2O4溶液和酸性KMnO4溶液反应生成二氧化碳、锰离子和水;
(2)据高锰酸钾呈酸性,盛放在酸式滴定管中来选择;
(3)根据滴定管的结构、精确度以及测量原理来解答;
(4)据滴定终点的判断是溶液中颜色的变化来分析;
(5)据此6H++5H2C2O4+2MnO4-=2Mn2++10CO2↑+8H2O离子方程式来计算;据滴定过程中眼睛应注视溶液中颜色变化,来判断滴定终点分析;根据 c(待测)=![]() 分析不当操作对V(标准)的影响,以此判断浓度的误差。
分析不当操作对V(标准)的影响,以此判断浓度的误差。
Ⅰ.实验①②是在相同浓度,不使用催化剂的条件下进行的,但反应温度不同,则为探究温度对速率的影响;而实验②④是在相同浓度、相同温度的条件下进行的,但②不使用催化剂,而④使用催化剂,则为探究催化剂对反应速率的影响;上述实验②③是探究浓度对化学反应速率的影响,则混合液的总体积必须相同,实验②溶液总体积为6mL,则实验③中所需水的体积a=25mL+4mL+2mL-25mL-4mL-1mL=1.0mL;反应速率需要通过时间的快慢来体现,则乙中需要测量的是溶液褪色所需时间,
故答案为:温度;1.0;溶液褪色所需时间;
Ⅱ.(1)H2C2O4溶液和酸性KMnO4溶液反应生成二氧化碳、锰离子和水,其反应的离子方程式为:6H++5H2C2O4+2MnO4-=2Mn2++10CO2↑+8H2O,
故答案为:6H++5H2C2O4+2MnO4-=2Mn2++10CO2↑+8H2O;
(2)高锰酸钾溶液呈酸性,应盛放在酸式滴定管中,
故答案为:b
(3)仪器A的名称是酸式滴定管;滴定管滴定前后读数为:0.80mL,20.80mL,消耗KMnO4溶液体积为20.80mL-0.80mL=20.00mL,滴定管下端有部分无刻度,滴定管内剩余的液体的体积大于大于29.1,故选D。
故答案为:20.00;D;
(4)据酸性KMnO4溶液为紫红色,滴定终点时无色变为紫红色,且半分钟不褪色为滴定到终点故眼睛应注视溶液中颜色变化,
故答案为:锥形瓶中颜色变色;溶液由无色变成紫红色,且半分钟内不褪色;
(5)
m(H2C2O4)=0.0025×90=0.225g; m(H2C2O4·xH2O )=1.26×![]() =0.315g; m(H2O)=0.315-0.225=0.09g;n(H2O)=
=0.315g; m(H2O)=0.315-0.225=0.09g;n(H2O)=![]() =0.005mol①
=0.005mol①
又因为 n H2C2O4)=0.0025 mol 根据元素守恒即n(H2C2O4·xH2O )=0.0025mol;n(H2O)=0.0025x②
联立①②得0.005=0.0025x,解得x=2;
未用标准KMnO4溶液润洗滴定管,溶液被稀释,造成V(标准)偏大,根据 c(待测)=![]() ,故c(待测)偏大,x偏小;
,故c(待测)偏大,x偏小;
故答案为:2;偏小。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】已知CO、H2和CO2组成的混合气体116.8 L(标准状况),经完全燃烧后放出的总能量为867.9 kJ,并生成18 g液态水。已知2H2(g)+O2(g)======2H2O(l)ΔH=-571.6 kJ·mol-1;2CO(g)+O2(g) ======2CO2(g) ΔH=-566 kJ·mol-1。则燃烧以前混合气体CO的体积分数最接近于 ( )
A.80%B.60%C.40%D.20%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A.新制的氯水放置一段时间,溶液的pH会减小
B.在配制硫酸亚铁溶液时往往要加入少量铁粉
C.恒容容器中反应CO(g)+NO2(g)![]() CO2(g)+NO(g) △H<0达到平衡后,升高温度,气体颜色变深
CO2(g)+NO(g) △H<0达到平衡后,升高温度,气体颜色变深
D.增大压强,有利于SO2与O2反应生成SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应:xA(气)+yB(气)![]() zC(气),达到平衡时测得A气体的浓度为0.5 mol.L-1,当在恒温下将该容器体积扩大一倍,再次达到平衡,测得A气体的浓度为0.3 mol.L-1,则下列叙述正确的是
zC(气),达到平衡时测得A气体的浓度为0.5 mol.L-1,当在恒温下将该容器体积扩大一倍,再次达到平衡,测得A气体的浓度为0.3 mol.L-1,则下列叙述正确的是
A. x+y<z B. 平衡向右移动
C. B的转化率升高 D. C的体积分数降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
A. 图1表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则等物质的量浓度的NaA和NaB混合溶液中:c(Na+)>c(A-)>c(B-)>c(OH-)>c(H+)
图1表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则等物质的量浓度的NaA和NaB混合溶液中:c(Na+)>c(A-)>c(B-)>c(OH-)>c(H+)
B.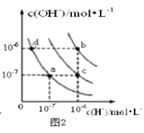 图2中在b点对应温度下,将pH=2的H2SO4溶液与pH=12的NaOH溶液等体积混合后,溶液显中性
图2中在b点对应温度下,将pH=2的H2SO4溶液与pH=12的NaOH溶液等体积混合后,溶液显中性
C.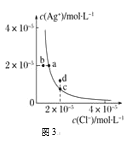 图3中d点没有AgCl沉淀生成
图3中d点没有AgCl沉淀生成
D.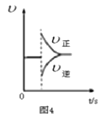 图4表示在N2(g)+3H2(g)
图4表示在N2(g)+3H2(g)![]() 2NH3(g)达到平衡后,减小NH3浓度时速率的变化
2NH3(g)达到平衡后,减小NH3浓度时速率的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作、现象和解释或结论都正确的是
选项 | 实验操作 | 现象 | 解释或结论 |
A | 过量的Fe粉中加入HNO3, | 溶液呈红色 | 稀HNO3将Fe氧化为 |
B | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
C | Al箔插入稀HNO3中 | 无现象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe3+与SCN-形成的配离子颜色极似血液,常被用于电影特技和魔术表演。回答下列问题:
(1)写出Fe3+的电子排布式:___________;SCN-的结构式为________
(2)基态硫原子中,核外占据最高能级电子的电子云轮廓图形状为_________。硫的一种同素异形体分子式为S8,其结构如图所示,其中S原子的杂化轨道类型为______。S8易溶于二硫化碳的原因是__________________________________________________。
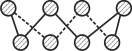
(3)已知立方氮化硼晶体内存在配位键,则其晶体中配位键与普通共价键数目之比为______。原子坐标参数可表示晶胞内部各原子的相对位置,图中a处B的原子坐标参数为(0, 0, 0),则距离该B原子最近的N原子坐标参数为_________。
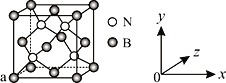
(4)单质铁的晶体结构如图所示,该堆积方式名称为________。已知该晶胞的密度为ρ g/cm3,则铁原子半径的计算式为______________ pm。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工艺的一个重要工序是铜洗,其目的是用铜液[醋酸二氨合铜(I)、氨水]吸收在生产过程中产生的CO和CO2等气体。铜液吸收CO的反应是放热反应,其反应方程式为: Cu(NH3)2Ac+CO+NH3![]() [Cu(NH3)3CO]Ac
[Cu(NH3)3CO]Ac
完成下列填空:
(1)如果要提高上述反应的反应速率,可以采取的措施是_________。(选填编号)
a 减压 b 增加NH3的浓度 c 升温 d 及时移走产物
(2)铜液中的氨可吸收二氧化碳,写出该反应的化学方程式__________
(3)铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为_________。其中氮元素原子最外层电子排布的轨道表达式是___________。通过比较_____________可判断氧,硫两种非金属元素的非金属性强弱。
(4)已知CS2与CO2分子结构相似,CS2的电子式是________。CS2熔点高于CO2,其原因是 ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,含Fe2O3等杂质)为原料冶炼铝的工艺如图:
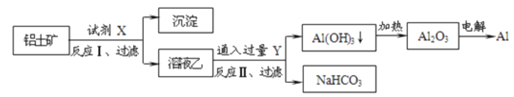
对上述流程判断正确的是( )
A.试剂X为稀硫酸或氢氧化钠溶液
B.反应II中生成Al(OH)3的反应为CO2+AlO2-+2H2O→Al(OH)3↓+HCO3-
C.结合质子(H+)的能力由强到弱的顺序是AlO2->OH->CO32->HCO3-
D.Al2O3熔点很高,工业上还可采用点解熔融AlCl3冶炼Al
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com