
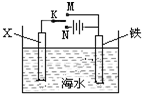
 已知海水中含有的离子主要有Na+、Mg2+、Cl-、Br-,利用右图装置进行实验探究,下列说法正确的是( )
已知海水中含有的离子主要有Na+、Mg2+、Cl-、Br-,利用右图装置进行实验探究,下列说法正确的是( )

 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源:2011-2012学年河北省石家庄市高三补充题、压轴题化学试卷(解析版) 题型:选择题
已知海水中含有的离子主要有Na+、Mg2+、Cl-、Br-,利用下图装置进行实验探究,下列说法正确的是()

A.X为锌棒,K置于M,可减缓铁的腐蚀,铁电极上发生的反应为2H++2e-=H2↑
B.X为锌棒,K置于M,外电路电流方向是从X到铁
C.X为碳棒,K置于N,可减缓铁的腐蚀,利用的是外加电流的阴极保护法
D.X为碳棒,K置于N,在X电极周围首先失电子的是Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:单选题


查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.X为锌棒,K置于M,可减缓铁的腐蚀,铁电极上发生的反应为2H++2e-=H2↑ |
| B.X为锌棒,K置于M,外电路电流方向是从铁到X |
| C.X为碳棒,K置于N,可减缓铁的腐蚀,利用的是外加电流的阴极保护法 |
| D.X为碳棒,K置于N,在X电极周围首先失电子的是Cl- |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年黑龙江省大庆实验中学高二(上)期末化学试卷(解析版) 题型:选择题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com