
| A、金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子 |
| B、氯化钠晶体中,每个Na+周围距离相等且最近的Na+共有6个 |
| C、金属晶体中,以“…ABCABCABC…”形式的堆积称为面心立方堆积 |
| D、干冰晶体中,每个CO2分子周围距离相等且最近的CO2分子共有12个 |


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
| A、Na2O2、HClO、SO2等物质都具有漂白作用 |
| B、液氨、液态氯化氢都是电解质 |
| C、置换反应都是氧化还原反应,复分解反应都是非氧化还原反应 |
| D、明矾能水解生成氢氧化铝胶体,可用作净水剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同 |
| B、同温同压下,H2(g)+Cl2(g)═2HCl(g) 在光照和点燃条件下的△H不同 |
| C、已知:①2H2(g)+O2(g)═2H2O(g)△H=-a kJ?mol-1,②2H2(g)+O2(g)═2H2O(l)△H=-b kJ?mol-1,则:a>b |
| D、已知:①C(s,石墨)+O2(g)═CO2(g)△H=-393.5 kJ?mol-1,②C(s,金刚石)+O2(g)═CO2(g)△H=-395.0 kJ?mol-1,则知:石墨比金刚石稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol Cl2常温下与过量NaOH溶液反应转移电子总数为 0.1NA |
| B、25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA |
| C、0.25mol Na2O2中含有的阴离子数为0.5 NA |
| D、1L 0.1mol?L-1的硫化钠溶液中硫离子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
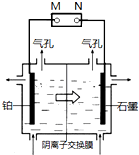 制备单质锰的实验装置如图,阳极以稀硫酸为电解液,阴极以硫酸锰和硫酸混合液为电解液,电解装置中箭头表示溶液中阴离子移动的方向.下列说法不正确的是( )
制备单质锰的实验装置如图,阳极以稀硫酸为电解液,阴极以硫酸锰和硫酸混合液为电解液,电解装置中箭头表示溶液中阴离子移动的方向.下列说法不正确的是( )| A、M是电源的负极 | ||||
| B、左侧气孔逸出的气体可能为副产物H2 | ||||
C、电解槽中发生的总反应为:MnSO4+2H2O
| ||||
| D、若用阳离子交换膜代替阴离子交换膜,阳极可能得到 MnO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤ | B、②④⑥ |
| C、②③④⑥ | D、①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 常温下,将pH和体积都相同的盐酸和醋酸溶液分别加蒸馏水稀释,pH随溶液体积变化如图,下列有关叙述正确的是( )
常温下,将pH和体积都相同的盐酸和醋酸溶液分别加蒸馏水稀释,pH随溶液体积变化如图,下列有关叙述正确的是( )| A、曲线I为醋酸稀释时pH值变化曲线 |
| B、a点时,若都加入相同大小的锌粒,此时盐酸反应的速率大 |
| C、a点时,若都加入足量的锌粒,最终与醋酸反应产生的氢气多 |
| D、b点溶液中水的电离程度比c点溶液中水的电离程度小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com