
| A、高温下用焦炭还原SiO2生产硅和一氧化碳属于置换反应 |
| B、BaSO4的水溶液不导电,故BaSO4是弱电解质 |
| C、元素的第一电离能越小,其金属性一定越强 |
D、化合物 可分为醇类、芳香烃类和羧酸类 可分为醇类、芳香烃类和羧酸类 |
 中羟基与苯环碳直接相连是酚类、芳香烃类只含碳和氢的组成的芳香族化合物.
中羟基与苯环碳直接相连是酚类、芳香烃类只含碳和氢的组成的芳香族化合物.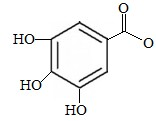 羟基与苯环碳直接相连是酚类、芳香烃类只含碳和氢的组成的芳香族化合物,还含有氧元素,故D错误;
羟基与苯环碳直接相连是酚类、芳香烃类只含碳和氢的组成的芳香族化合物,还含有氧元素,故D错误;

科目:高中化学 来源: 题型:
| A、农作物收获后,就地焚烧秸秆,增加土壤中钾肥含量 |
| B、厨房中燃气泄漏,立即打开抽油烟机排气 |
| C、硝酸是重要的工业原料,可用于制造炸药 |
| D、高纯硅可用于制作光导纤维,光导纤维遇强碱会“断路” |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滤液b的pH=7 |
| B、②中颜色变化说明Mg(OH)2转化为Fe(OH)3 |
| C、实验可以证明Fe(OH)3的溶解度比Mg(OH)2的小 |
| D、浊液a中存在沉淀溶解平衡:Mg(OH)2(s)?Mg2+(aq)+2OH-(aq) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解精炼铜时,若转移了NA个电子,则阴极析出32g铜 |
| B、标准状态下,33.6L氟化氢中含有1.5NA个氟化氢分子 |
| C、0.1mol/L的Al2(SO4)3溶液中,Al3+的数目小于0.2NA |
| D、1mol FeCl3跟水反应,完全转化为氢氧化铁胶体后,其中胶体粒子的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(OH-) |
| c(H+) |
| A、该一元酸溶液的pH=1 | ||
| B、该溶液中HA的电离度为1% | ||
| C、该溶液中水的离子积常数为1×10-22 | ||
D、若加水稀释,则
|
查看答案和解析>>
科目:高中化学 来源: 题型:
A、在稀氨水中通入过量CO2:NH3?H2O+CO2=N
| ||||
| B、少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO | ||||
C、向Ba(OH)2溶液中加入少量的NaHSO3溶液2HS
| ||||
| D、氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-=CaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
2- 3 |
| A、上述反应中的氧化剂是Cl2 |
| B、该反应过程中只有氮元素被氧化 |
| C、还原性:CN->Cl- |
| D、当有1 molCl2参加反应时,转移的电子数为2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 钠 | Na2CO3 | 金刚石 | 石墨 | |
| 熔点(℃) | 97.8 | 851 | 3550 | 3850 |
| 沸点(℃) | 882.9 | 1850(分解产生CO2) | ---- | 4250 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com