
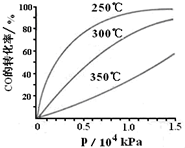
 科学家利用太阳能分解水生成氢气,再用氢气与二氧化碳在催化剂作用下反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知:
科学家利用太阳能分解水生成氢气,再用氢气与二氧化碳在催化剂作用下反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知:| 1 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 702.1 |
| 726.5 |


科目:高中化学 来源: 题型:
| A、含有AlO2-的溶液中:Na+、Al3+、NO3-、Cl- |
| B、使淀粉碘化钾变蓝的溶液中:K+、HCO3-、S2-、SO42- |
| C、能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、Na+ |
| D、通有SO2的溶液中:Fe2+、Mg2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(B+)>c(A-)>c(OH-)>c(H+) |
| B、c(A-)>c(B+)>c(H+)>c(OH-) |
| C、c(B+)=c(A-)>c(H+)=c(OH-) |
| D、c(B+)>c(A-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、③④ | C、②③ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 试剂Z | 离子X | 离子Y |
| A.NH3.H2O B.AgNO3 C.Na2SO4 D.Ba(NO3)2 | Al3+ Cl- Ba2+ SO42- | Mg2+ CO32- Mg2+ Cl- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1 | B、3:7 |
| C、7:3 | D、81:77 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色 |
| B、欲除去Cl2中少量HCl气体,可将此混合气体通过盛饱和食盐水的洗气瓶 |
| C、漂白粉有效成分是CaCl2和Ca(ClO)2,应密闭保存 |
| D、SO2和Cl2都具有漂白作用,所以将两种气体同时作用于潮湿有色物质,可大大增强漂白作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com