
| 时间 (s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO) (×10-4,mol/L) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO) (×10-3,mol/L) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
分析 (1)根据△G=△H-T•△S<0能自发进行判断;
(2)计算出NO的反应速率,根据反应速率与化学计量数的关系可计算v(N2),计算出平衡时各物质的浓度,可计算平衡常数;
(3)反应的平衡常数表达式:K=$\frac{生成物平衡浓度系数次幂之积}{反应物平衡浓度系数次幂之积}$;
(4)能提高NO转化率,应使平衡向正向移动,结合温度、浓度等外界条件对平衡移动的影响解答.
解答 解:(1)由反应能够自发进行,则△H-T△S<0,由方程式可知△S<0,则只有该反应的△H<0时,即该反应一定是放热才有可能自发进行,
故答案为:放热;
(2)前3s内的平均反应速率v(N2)=$\frac{1}{2}$v(N0)=$\frac{1}{2}$×$\frac{10.0×1{0}^{-4}mol/L-1.50×1{0}^{-4}mol/L}{3s}$=1.42×10-4 mol•L-1•S-1,
(3)反应 2NO+2CO $\frac{\underline{\;催化剂\;}}{\;}$2CO2 +N2的K=$\frac{{c}^{2}(C{O}_{2})×c({N}_{2})}{{c}^{2}(NO)×{c}^{2}(CO)}$,故答案为:$\frac{{c}^{2}(C{O}_{2})×c({N}_{2})}{{c}^{2}(NO)×{c}^{2}(CO)}$;
(4)a.选用更有效的催化剂,不能使平衡发生移动,故错误;
b.升高反应体系的温度,因反应放热,则平衡逆向移动,转化率减小,故错误;
c.降低反应体系的温度,平衡正向移动,转化率增大,故正确;
d.缩小容器的体积,平衡正向移动,转化率增大,故正确,
故答案为:cd.
点评 本题考查较为综合,涉及盖斯定律的应用、平衡移动的影响以及相关计算,侧重于学生的分析能力、计算能力的考查,为高考常见题型,难度较大.


科目:高中化学 来源: 题型:多选题
| A. | 丙烷 | B. | 丙烯 | C. | 1,3-丁二烯 | D. | 乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
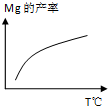 除电解法,工业炼镁还可采用硅热法(Pidgeon法).即以煅白(CaO•MgO)为原料与硅铁(含硅75%的硅铁合金)混合置于密闭还原炉,1200℃下发生反应:2(CaO•MgO)(s)+Si(s)?Ca2SiO4 (l)+2Mg(g)
除电解法,工业炼镁还可采用硅热法(Pidgeon法).即以煅白(CaO•MgO)为原料与硅铁(含硅75%的硅铁合金)混合置于密闭还原炉,1200℃下发生反应:2(CaO•MgO)(s)+Si(s)?Ca2SiO4 (l)+2Mg(g)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:X>Y>Z | |
| B. | 气态氢化物稳定性按X、Y、Z依次减弱 | |
| C. | 非金属性:X>Y>Z | |
| D. | 阴离子还原性:X-<Y2-<Z3- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.50 mol | B. | 0.75 mol | C. | 1.00 mol | D. | 1.50 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液I中含有溶质的组合可能有4种 | |
| B. | 已知V和a的具体数值可以确定溶液I的溶质 | |
| C. | 已知溶液I中溶质的种类和a值,一定能求出V | |
| D. | 向溶液I中加入足量Ba(OH)2溶液充分反应后,过滤出沉淀,经烘干得固体质量为W克.由W和V的值可确定溶液I的溶质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室常用如图所示的简易装置进行NO气体的制备和收集
实验室常用如图所示的简易装置进行NO气体的制备和收集查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com