
| A. | 1 mol H2和0.5 mol O2反应放出的热量就是H2的燃烧热 | |
| B. | 等质量的硫蒸气和硫固体分别完全燃烧,相同条件下,前者放出的热量多 | |
| C. | 水中的钢闸门连接电源的负极,属于外加电流的阴极保护法 | |
| D. | 铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀 |
分析 A.氢气的燃烧热是1mol氢气燃烧生成1mol液态水时放出的热量;
B.等质量的同种物质,气态时具有的能量高;
C.与负极相连作阴极,阴极被保护;
D.铁遇浓硝酸会在铁的表面形成致密的氧化膜.
解答 解:A.氢气的燃烧热是1mol氢气燃烧生成1mol液态水时放出的热量,没有说明生成物水的状态,所以不一定是燃烧热,故A错误;
B.等质量的硫蒸气和硫固体,硫蒸气具有的能量高,所以分别完全燃烧,相同条件下,前者放出的热量多,故B正确;
C.水中的钢闸门连接电源的负极,钢闸作阴极,阴极被保护,属于外加电流的阴极保护法,故C正确;
D.铁遇浓硝酸会在铁的表面形成致密的氧化膜,可保护内部不被腐蚀,故D正确.
故选A.
点评 本题考查了燃烧热、物质状态与能量的关系、金属的电化学防护、铁的性质,题目难度不大,注意相关知识的积累,侧重于考查学生对基础知识的应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年河南省新乡市高二上第一次月考化学卷(解析版) 题型:选择题
在一个不导热的密闭反应器中,只发生两个反应:
a(g)+b(g)  2c(g) ΔH1<0
2c(g) ΔH1<0
x(g)+3y(g)  2z(g)ΔH2>0
2z(g)ΔH2>0
进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是( )
A.等压时,通入惰性气体,c的物质的量不变
B.等压时,通入z气体,反应器中温度升高
C.等容时,通入惰性气体,各反应速率不变
D.等容时,通入z气体,y的物质的量浓度增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆市高二上第一次月考化学卷(解析版) 题型:选择题
常温下,下列有关电解质溶液的说法正确的是
A.pH=3的强酸溶液1ml,加水稀释至100ml后,溶液pH降低2个单位
B.0.2molCO2通入1L0.3mol·L-1 KOH溶液中:2c(H+)+ c(HCO3-)+ 3c(H2CO3)=2c(OH-)+c(CO32-)
C.已知一定浓度的NaHSO3溶液pH=5.4,则c(Na+)>c(HSO3-)>c(H2SO3)>c(SO32-)
D.pH相同的①CH3COONa ②NaHCO3③NaClO三种溶液中的c(Na+):①<②<③
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 几种物质都有 | B. | 有甲酸乙酯,可能有甲酸 | ||
| C. | 有甲酸乙酯和甲醇 | D. | 有甲酸乙酯,可能有甲醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
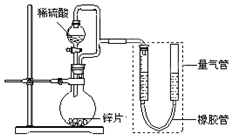 某同学设计了如图所示装置(部分夹持装置已略去),该装置可以用来进行多项实验研究.
某同学设计了如图所示装置(部分夹持装置已略去),该装置可以用来进行多项实验研究.| 序号 | V(H2SO4)/mL | c(H2SO4)/mol•L-1 | t/s |
| Ⅰ | 40 | 1 | t1 |
| Ⅱ | 40 | 4 | t2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4NH3(g)+5O2(g)═4 NO(g)+6 H2O(g)△H=+a kJ•mol-1 | |
| B. | C6H12O6(s)+6O2(g)═6CO2(g)+6H2O(l)△H=-b kJ•mol-1 | |
| C. | 2CO(g)+O2(g)═2CO2(g)△H=-c kJ•mol-1 | |
| D. | CH3CH2OH(l)+$\frac{1}{2}$O2(g)═CH3CHO(l)+H2O(g)△H=-d kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
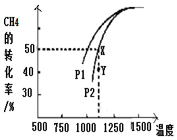 研究含氮、硫污染物的治理是环保的一项重要工作.
研究含氮、硫污染物的治理是环保的一项重要工作.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤ | B. | ②③⑥⑦ | C. | ④⑦ | D. | ⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com