
【题目】碳、氢元素可形成种类繁多的烃类物质。
(1)下图表示某些烃分子的模型:
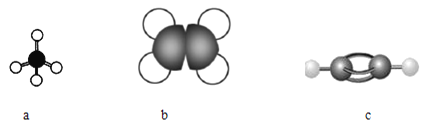
①写出a分子的空间构型______。
②c分子中的一个氢原子被![]() —取代后的物质共直线的原子最多有______个。
—取代后的物质共直线的原子最多有______个。
③取等质量的上述三种烃充分燃烧,耗氧量最大的是______(填分子式)。
④25℃和101kPa时,取a、b和c组成的混合烃32mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了56mL,原混合烃中c的体积分数为______。
(2)某烯烃的结构简式如下所示:
![]()
①用系统命名法对该烃与![]() 的加成产物命名:______,该加成产物的—氯取代物有______种。
的加成产物命名:______,该加成产物的—氯取代物有______种。
②该烯烃可以加聚生成高分子,写出该高聚物的结构简式______。该烯烃还能与乙烯以1:1比例反应形成一种环状化合物,请写出该环状化合物的键线式______。
【答案】正四面体 6 ![]() 50% 2-甲基丁烷 4
50% 2-甲基丁烷 4 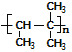
【解析】
根据球棍模型和比例模型可知,a为甲烷,b为乙烯,c为乙炔,以此分析。
(1) ①甲烷是正四面体;
②乙炔分子四原子共直线,苯分子中存在对顶角两个碳原子和两个氢原子共四原子共直线,所以乙炔分子中的一个氢原子被C6H5—取代后的物质共直线的原子最多有6个;
③等质量的烃含氢质量分数越大,耗氧量越大,所以等质量的甲烷、乙烯和乙炔充分燃烧,耗氧量最大的是CH4;
④25℃和101kPa时,根据烃CxHy燃烧通式,
CxHy+(x+![]() )O2→xCO2+
)O2→xCO2+![]() H2O △V
H2O △V
1 x+![]() x 1+
x 1+![]()
32mL 56mL
![]() =
=![]() ,解得y=3,因为CH4和C2H4都含有4个碳原子,C2H2含有2个碳原子,设C2H2所占的体积分数为x,则CH4和C2H4占(1-x),所以4(1-x)+2x=3,解得x=0.5,即原混合烃中c的体积分数为50%;
,解得y=3,因为CH4和C2H4都含有4个碳原子,C2H2含有2个碳原子,设C2H2所占的体积分数为x,则CH4和C2H4占(1-x),所以4(1-x)+2x=3,解得x=0.5,即原混合烃中c的体积分数为50%;
因此,本题正确答案为:正四面体;6;CH4;50%;
(2) ①该烃为烯烃,与H2的加成产物为烷烃,主链有四个碳原子,甲基为支链位于主链上第二个碳原子上,故命名为2-甲基丁烷,该烷烃有四种类型的氢原子,所以—氯取代物有4种;
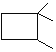
②该烯烃可以加聚生成高分子,高聚物的结构简式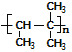 ;该烯烃与乙烯以1:1比例反应形成一种环状化合物,要断开双键形成环,故该环状化合物的键线式为
;该烯烃与乙烯以1:1比例反应形成一种环状化合物,要断开双键形成环,故该环状化合物的键线式为 。
。
因此,本题正确答案为:2-甲基丁烷;4;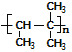 ;
; 。
。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】现有短周期主族元素X、Y、Z、R、T。R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡,五种元素的原子半径与原子序数的关系如图所示,下列推断正确的是

A. 原子半径和离子半径均满足:Y<Z
B. Y的单质易与R、T的氢化物反应
C. 最高价氧化物对应的水化物的酸性:T<R
D. 由X、R、Y、Z四种元素组成的化合物水溶液一定显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能达到实验目的或得出相应结论的是
实 验 操 作 | 目的或结论 | |
A | 将Cu片放入FeCl3溶液中 | 证明Fe的金属性比Cu强 |
B | 将点燃的镁条置于盛有CO2的集气瓶中,瓶内壁有黑色固体生成 | 镁与CO2发生置换反应 |
C | 将SO2通入溴水或酸性高锰酸钾溶液中 | 证明SO2有漂白性 |
D | 向FeCl2溶液(含少量FeBr2杂质)中,加入适量氯水,再加CCl4萃取分液 | 除去FeCl2溶液中的FeBr2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.含有1mol原子的氢气在标准状况下的体积约为22.4 L
B.25 ℃,1.01×105Pa,64 g SO2中含有的原子数为3NA
C.1 mol/L的Na2SO4溶液含Na+数为2 NA
D.标准状况下,11.2 L H2O含有的分子数为9 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求书写下列化学方程式。
(1)铁和高温水蒸气反应的化学方程式:____________。
(2)向NaHCO3溶液中加入NaOH溶液的离子方程式:___________。
(3)Al2(SO4)3的电离方程式:_____________。
(4)钠和氧气在加热条件下反应的化学方程式:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2CO3是重要的化工原料,工业上采用NH3、CO2、NaCl为原料来制备。某兴趣小组用NH4HCO3固体替换NH3和CO2,按照下列流程在实验室模拟制备Na2CO3。

完成下列填空:
(1)步骤1中,为控制反应温度在30~35℃,应选用的加热方式是_______________;实验前NH4HCO3固体须在____________里(填仪器名称)磨成粉末,且加入时要不断搅拌,这些操作的目的是_____________________________________________________________。
(2)步骤3中,使用饱和NaHCO3溶液洗涤白色固体的原因是____________________________。
(3)步骤4中,恒温炉内发生的化学反应为______________________________(书写化学方程式)。
为检验产品纯度,该小组按如下流程操作:

(4)判断操作II中滴加Ba(OH)2溶液是否过量的方法是___________________________________。
(5)若样品中杂质不与Ba(OH)2反应,则Na2CO3的质量分数为____________(小数点后保留两位)。
(6)若样品中所含杂质是NaHCO3、NaCl中的一种或两种,①如何确定样品中是否含有NaCl,设计实验方案_________________________________________________________________。
②有同学认为,根据上述实验数据就可以判断出样品中一定含有NaCl,无需再实验检验,判断的理由是____________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设计如图装置研究电化学反应,a、b可用导线连接。下列叙述错误的是

A. a、b不连接时,铁片上有气泡产生
B. a、b连接时,铜片上发生反应:2H++2e→H2↑
C. a、b连接时,溶液中产生电子的定向移动
D. 无论a和b是否连接,铁片上都会发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是原子序数依次增大的五种短周期主族元素,其中A的原子序数是B和D原子序数之和的1/4,C的原子半径在所有短周期主族元素中最大,甲和丙是D元素的两种常见氧化物,乙和丁是B元素的两种常见同素异形体,0.005 mol/L戊溶液的pH=2,它们之间的转化关系如图所示(部分反应物省略),下列叙述一定正确的是
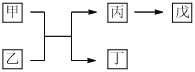
A. C、D两元素形成的化合物的原子个数比为1:2
B. C、E形成的化合物的水溶液呈碱性
C. 简单离子半径:D> C> B
D. 最高价氧化物对应水化物的酸性:E>A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学家们合成了如图所示的一系列的星烷,如三星烷、四星烷、五星烷等。下列说法正确的是


A. 它们之间互为同系物
B. 六星烷的化学式为C18H22
C. 三星烷与丙苯互为同分异构体,四星烷与 互为同分异构体
互为同分异构体
D. 它们的一氯代物均只有两种而三星烷得二氯代物有四种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com