
| A、门捷列夫 | B、道尔顿 |
| C、卢瑟福 | D、汤姆孙 |


科目:高中化学 来源: 题型:
| A、Cl2是还原产物 |
| B、HCl全部被还原 |
| C、KMnO4被氧化 |
| D、HCl既表现还原性又表现酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①④⑤ | B、②⑤⑥ |
| C、③⑤⑥ | D、⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCO3与盐酸反应制CO2:CaCO3+2H+→Ca2++H2O+CO2↑ | ||
B、实验与浓硫酸反应制HCl:H2SO4(浓)+Cl-
| ||
C、电解熔融的氯化钠:2Cl-+2H2O
| ||
| D、Ba(OH)2与小苏打恰好完全反应:Ba2++HCO3-→BaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH |
| B、Zn |
| C、Fe |
| D、NH3?H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
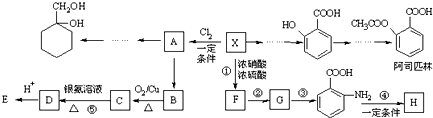
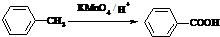
 (苯胺,易被氧化)
(苯胺,易被氧化)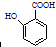 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有 和其他无机物合成
和其他无机物合成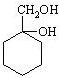 最合理的方案(不超过4步).
最合理的方案(不超过4步).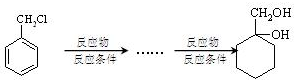
查看答案和解析>>
科目:高中化学 来源: 题型:
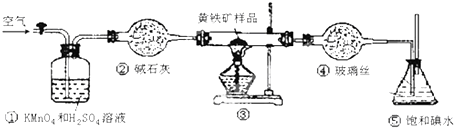
| 滴定次数 | 待测液体的体积/mL | 标准碱溶液的体积/mL | |
| 滴定前 | 滴定后 | ||
| 第一次 | 20.00mL | 0.00 | 20.58 |
| 第二次 | 20.00mL | 0.22 | 20.20 |
| 第三次 | 20.00mL | 0.36 | 20.38 |
查看答案和解析>>
科目:高中化学 来源: 题型:
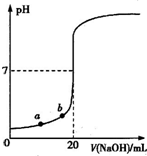
| A、水电离出的氢离子浓度:a>b |
| B、盐酸的物质的量浓度为0.0100mol?L-1 |
| C、指示剂变色时,说明盐酸与NaOH恰好完全反应 |
| D、当滴加NaOH溶液10.00mL时,该混合液的pH=1+lg3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com