
| ��ѧ��Ӧ | ƽ�ⳣ�� | �¶ȣ��棩 | |
| 500 | 800 | ||
| ��2H2��g��+CO��g��?CH3OH��g�� | K1 | 2.5 | 0.15 |
| ��H2��g��+CO2��g��?H2O ��g��+CO��g�� | K2 | 1.0 | 2.50 |
| ��3H2��g��+CO2��g��?CH3OH��g��+H2O ��g�� | K3 | ||
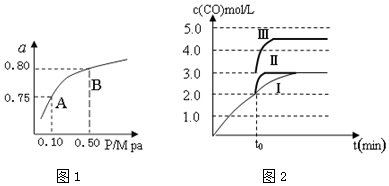
���� ��1������ͼ�����ݣ���Ӧ��ƽ�ⳣ�����¶���������ƽ��������У�����Ӧ�����ȷ�Ӧ��
��2������ƽ�ⳣ�����¶ȱ仯������ѹǿ�仯������
��3�����ݷ�Ӧ��+�ڵõ���Ӧ�ۣ�����ƽ�ⳣ��K3=K1��K2�����㲻ͬ�¶��·�Ӧ�۵�ƽ�ⳣ��������¶ȱ仯�����жϷ�Ӧ�ʱ䣻
��4��ͼ��������ߢ�仯Ϊ���ߢ������̷�Ӧ�ﵽƽ���ʱ�䣬���ﵽ��ͬƽ��״̬������ǿɱ���Ǻ�ѹ������˵���ı���Ǽ����˴����������ߢ��Ϊ���ߢ�ʱһ����̼���ʵ�������Ӧ�������������ķ�Ӧ���ɱ����������������Ũ�ȳɷ��ȣ��������ʵ������䣮
��� �⣺��1������ͼ�����ݣ���Ӧ��ƽ�ⳣ�����¶���������ƽ��������У�����Ӧ�����ȷ�Ӧ��
�ʴ�Ϊ�����ȣ�
��2������ƽ�ⳣ�����¶ȱ仯������ѹǿ�仯������ͼ����ƽ��״̬��A�䵽Bʱ��ѹǿ�ı䣬�¶Ȳ��䣬����ƽ�ⳣ�����䣬
�ʴ�Ϊ��=��
��3�����ݷ�Ӧ��+�ڵõ���Ӧ�ۣ�����ƽ�ⳣ��K3=K1��K2����Ӧ�۵�ƽ�ⳣ����500��Cʱ��K3=K1��K2=2.5��1.0=2.5��500��Cʱ��K3=K1��K2=2.5��1.0=2.5��800��Cʱ��K3=K1��K2=2.5��0.15=0.375������¶ȱ仯���������¶����ߣ�ƽ�ⳣ����С��ƽ��������У������жϷ�Ӧ�Ƿ��ȷ�Ӧ���ʱ��H��0��
��500�桢2L���ܱ������У����з�Ӧ�ۣ����ijʱ��H2��CO2��CH3OH��H2O�����ʵ����ֱ�Ϊ6mol��2mol��10mol��10mol��Q=$\frac{5��5}{{3}^{3}��1}$=0.93��K=2.5����Ӧ������У�V����V�棻
�ʴ�Ϊ��2.5����������
��4��ͼ��������ߢ�仯Ϊ���ߢ������̷�Ӧ�ﵽƽ���ʱ�䣬���ﵽ��ͬƽ��״̬������ǿɱ���Ǻ�ѹ������˵���ı���Ǽ����˴����������ߢ��Ϊ���ߢ�ʱһ����̼���ʵ�������Ӧ�������������ķ�Ӧ���ɱ����������������Ũ�ȳɷ��ȣ��������ʵ������䣬���ߢ����Ϊ3L��һ����̼Ũ��Ϊ3mol/L���ı���������Ϊ���ߢ�һ����̼Ũ��Ϊ4.5mol/L�������ѹ�����Ϊ��3��V=4.5��3��V=2L�����Խ��������������ѹ����2L���ϣ�
�ʴ�Ϊ��������������������������ѹ����2L��
���� ���⿼����ƽ�ⳣ�������Ӱ��������Ӧ�á�ƽ��ͼ��ķ���Ӧ�á���Ӧ�ȵ��жϵȣ���Ŀ�ۺ��Խϴ����ڿ���ѧ���ķ��������ͼ���������ע�����ƽ�ⳣ���ļ����Լ�Ӧ��Qc�ж�ƽ���ƶ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ǽ���������һ���������������� | |
| B�� | ����������һ�����ǽ��������� | |
| C�� | �������ᷴӦ������Ӧ������һ���������� | |
| D�� | ������ԭ��Ӧһ���������ӷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Sr��OH��2�ܽ���ˮ | B�� | SrSO4������ˮ | ||
| C�� | BaSO4������ˮ | D�� | Ba��OH��2��Ca��OH��2��������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
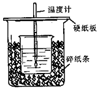 ��50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��ش��������⣺
��50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ͻ�����̼ԭ�Ӳ��ܷ�����ѧ��Ӧ | |
| B�� | Cԭ��ֻ����Cԭ���γɲ����ͼ� | |
| C�� | �κ��л�����Hԭ����Ŀ������Ϊ���� | |
| D�� | ���Cԭ��֮���ܹ��γ����̼̼���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������һ�ֳ��õĻ�ԭ�������û�ѧ����ʽ��ʾ���ڹ�ҵ�ϵ�һ����Ҫ��;��3CO+Fe2O3$\frac{\underline{\;\;��\;\;}}{\;}$2Fe+3CO2��
������һ�ֳ��õĻ�ԭ�������û�ѧ����ʽ��ʾ���ڹ�ҵ�ϵ�һ����Ҫ��;��3CO+Fe2O3$\frac{\underline{\;\;��\;\;}}{\;}$2Fe+3CO2���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 672 mL | B�� | 168 mL | C�� | 504 mL | D�� | 224 mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com