
【题目】反应N2O4(g)2NO2(g)△H=+57kJmol﹣1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示.下列说法正确的是
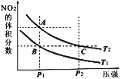
A. A、C两点的反应速率:A>C
B. A、C两点气体的颜色:A深,C浅
C. A、B两点气体的平均相对分子质量:A>B
D. B、C两点化学平衡常数:B<C
【答案】D
【解析】
A、A、C两点温度相同,C点压强大于A点,所以C点反应速率大于A点反应速率,A错误;B、C点压强大于A点压强,所以C点容器体积小于A 点容器体积,所以C点NO2的浓度大于A点NO2的浓度,C点颜色深,A点浅,B错误;C、A、B两点压强相同,B点到A点NO2体积分数增大,平衡正向移动,气体的总物质的量增大,又由于气体的总质量不变,所以混合气体的平均相对分子质量减小,即A、B两点气体的平均相对分子质量:B > A,C错误;D、A、B两点压强相同,B点到A点NO2体积分数增大,平衡正向移动,所以B点的平衡常数小于A点的平衡常数,A、C两点温度相同,A、C两点平衡常数相同,所以B点的平衡常数小于C点的平衡常数,D正确。正确答案为D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】石油化工是江苏省的支柱产业之一。醋酸乙烯酯是合成维尼纶的重要单体,某化工厂曾利用下列工艺生产醋酸乙烯酯:
2CH2=CH2+O2![]() 2CH3CHO………………………………………①
2CH3CHO………………………………………①
2CH3CHO+O2![]() 2CH3COOH……………………………………………②
2CH3COOH……………………………………………②
2CH2=CH2+2CH3COOH+O2→2CH3COOCH=CH2+2H2O…………………③
由于副反应的发生,反应①中乙烯的利用率为75%,反应②中乙醛的利用率为80%,反应③中乙烯和乙酸的利用率均为75%。
(1)为使乙酸乙烯酯获得最大产量,乙烯先后两次的投料比为多少_______?
(2)以2.8×104kg 乙烯为原料最多可制得醋酸乙烯酯多少千克_______?
(3)若各步副反应中反应物物质的量之比均与主反应相同。以乙烯和空气为原料生产醋酸乙烯酯,通入的空气(O2的体积分数为1/5)与乙烯的体积比至少为多少_______?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知气态烃A的密度是相同状况下氢气密度的14倍,有机物A-E能发生下图所示一系列变化,则下列说法错误的是( )
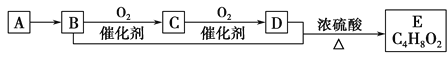
A. A分子中所有原子均在同一平面内
B. C4H8O2含酯基的同分异构体有6种
C. D可与Na2CO3溶液反应
D. 等物质的量的B、D与足量钠反应生成气体的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲图是部分短周期元素的常见化合价与原子序数的关系图:
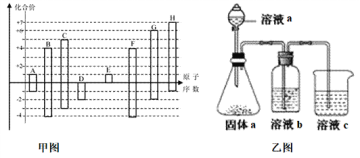
请回答下列问题:
(1)D元素在周期表中的位置为___________,D和G的简单氢化物中沸点高的是___________(写化学式),A和E形成的化合物的电子式为_____________。
(2)D、E、G、H的简单离子半径由大到小的顺序为__________________________。(用化学式表示)
(3)H的最高价氧化物对应的水化物的浓溶液不稳定,受热可分解,产物之一是H的单质,且当有28mol电子转移时,常温共产生9mol气体,写出该反应的化学方程式_________________。
(4)由上述元素中的几种组成a、b、c各物质,某同学设计实验用乙图装置证明元素B、C、F的非金属性强弱(其中溶液b和溶液c均为足量)。
①溶液a和b分别为________,________(填化学式)。
②溶液c中的离子方程式为__________________________________________。
③请从原子结构的角度解释非金属性C>B的原因____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常溫下,浓度均为1.0mol/L的HX溶液、HY溶液、HY和 NaY的混合溶液,分别加水稀释,稀释后溶液的pH随浓度的变化如图所示,下列叙述正确的是( )

A. HX是强酸,溶液每稀释10倍,pH始终增大1
B. 常温下HY的电离常数为1.0×10-4
C. 溶液中水的电离程度:a点大于b点
D. c 点溶液中:c(Na+)>c(Y-)>c(HY)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“电化学”与人类生产和生活密不可分。
(1)如图为相互串联的甲、乙两个电解池,试回答下列问题。
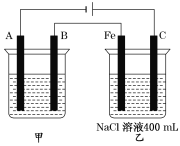
①甲池若为用电解原理精炼铜的装置,A极电极反应式为___________。
②乙池中若滴入少量酚酞溶液,开始一段时间后,____电极附近呈红色(填“铁”或“碳”)。
③甲池若为用电解原理精炼铜的装置,阴极增重12.8 g时,则乙池阳极放出气体在标准状况下的体积为________(不考虑气体溶解情况)。
(2)肼(N2H4)—空气燃料电池是一种环境友好型碱性电池,该电池放电时,负极的反应式为_______。
(3)人工肾脏可用电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图。
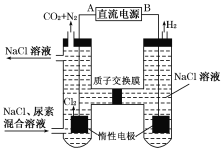
①阳极反应生成的氯气将尿素氧化而得以除去,试写出该反应的化学方程式________________。
②电解结束后,阴极室溶液的pH与电解前相比将________(填增大、减小或不变);若两极共收集到气体13.44 L(标况),则除去的尿素为________ g(忽略气体的溶解)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知烯烃在臭氧作用下,双键断裂如下:

(1)判断下列有机物经臭氧化分解的产物
①![]() ______________________________________________________________
______________________________________________________________
②![]() _____________________________________________________________________
_____________________________________________________________________
③![]() ________________________________________________________
________________________________________________________
(2)如果二甲苯也能发生臭氧化分解,则判断邻二甲苯的臭氧化分解产物_______________________________
(3)若烯烃A(C8H16)经臭氧化分解后仅得一种化合物B,B经催化氢化后生成醇C(C4H10O),C用浓H2SO4处理后只生成一种无侧链的烯烃D(C4H8),则A的结构简式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知α—氨基酸在一定条件下能与亚硝酸HNO2反应得到α—羟基酸。
![]()
根据如下转化关系回答下列问题:
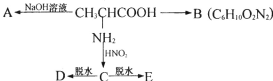
其中D、E的摩尔质量分别为162gmol-1、144gmol-1。
(1)写出A、B的结构简式A___________________、B______________________。
(2)写出C→E的化学方程式___________________________________________。
(3)写出C→D的化学方程式___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知空气—锌电池的电极反应为
锌片:Zn+2OH2e===ZnO+H2O;
碳棒:O2+2H2O+4e===4OH,据此判断,锌片是
A. 正极,被还原B. 正极,被氧化C. 负极,被还原D. 负极,被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com