
��800��ʱ�����ݻ�Ϊ2L�ĺ����ܱ������г���һ������CO��H2Oά�ֺ��£�������ӦCO(g)+H2O(g) H2(g)+CO2(g)����Ӧ�����вⶨ�IJ������ݼ��±���
H2(g)+CO2(g)����Ӧ�����вⶨ�IJ������ݼ��±���
| ��Ӧʱ��/min | 0 | 2 | 4 | 6 |
| n(CO)/mol | 1.20 | 0.90 | | 0.80 |
| n(H2O)/ mol | 0.60 | | 0.20 | |
| ��� | ҩƷ1 | ҩƷ2 | ʵ������ |
| I | 0.01 mol/L NaOH��Һ | 0.01 mol/L MgCl2��Һ | ���ɰ�ɫ���� |
| II | 0.01 mol/L��ˮ | 0.01 mol/L MgCl2��Һ | ������ |
| III | 0.1 mol/L��ˮ | 0.1 mol/L MgCl2��Һ | ����III |
| IV | 0.1 mol/L��ˮ | 0.01 mol/L MgCl2��Һ | ���ɰ�ɫ���� |
| V | 0.01 mol/L��ˮ | 0.1 mol/L MgCl2��Һ | ������ |
 2NH4+(aq) + Mg(OH)2(s)�÷�Ӧ��ѧƽ�ⳣ���ı���ʽΪK= ���г��÷�Ӧƽ�ⳣ��K��Kb(NH3��H2O)��Ksp(Mg(OH)2)�Ĺ�ϵʽ ��
2NH4+(aq) + Mg(OH)2(s)�÷�Ӧ��ѧƽ�ⳣ���ı���ʽΪK= ���г��÷�Ӧƽ�ⳣ��K��Kb(NH3��H2O)��Ksp(Mg(OH)2)�Ĺ�ϵʽ �� ����15�֣��� ��0.075 mol��L��1��min��1��2�֣� ��1��2�֣� ������(1��)
�� ��2�֣�
��2�֣�
�� �����ɰ�ɫ������2�֣� ��4��10-5 mol��L��1��2�֣���K�� ��
��
K��Kb2/Ksp����2�֣�
���������������.�ٸ��ݱ������ݿ�֪����Ӧ��2 minʱCO�����ʵ���������1.20mol��0.90mol��0.30mol�����ݷ���ʽ��֪��ˮ���������ʵ���Ҳ����0.30mol����Ũ����0.30mol��2L��0.15mol/L������2min�ڵ�ƽ������Ϊv(H2O)�� ��0.075 mol��L��1��min��1��
��0.075 mol��L��1��min��1��
��2minʱˮ���������ʵ�����0.30mol��3minʱ��0.20mol������0.10mol����3minʱCO�����ʵ�����0.80mol������4minʱCO�����ʵ���Ҳ��0.8mol����˵����Ӧ��3minʱ�ﵽƽ��״̬����
CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
��ʼŨ�ȣ�mol/L�� 0.60 0.30 0 0
ת��Ũ�ȣ�mol/L�� 0.20 0.20 0.20 0.20
ƽ��Ũ�ȣ�mol/L�� 0.40 0.10 0.20 0.20
����ƽ�ⳣ��K�� ��1.0
��1.0
�۱��������������䣬��ƽ����ϵ����ͨ��0.20 mol H2O������ˮ������Ũ�ȣ�ƽ��������Ӧ������У����CO��ת��������
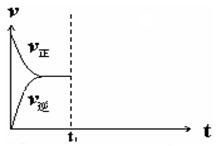
��ά���¶���ѹǿ���䣬t1ʱ��ͨ���1 mol��CO��H2O�Ļ�����壬���������ݻ���Ȼ�������ڷ�Ӧǰ��������䣬����ƽ���ǵ�Ч�ġ�������Ӧ���������淴Ӧ���ʼ�С����ƽ��״̬���䣬�����ȷ��ͼ���� ��
��
�� �ٸ��ݱ������ݿ�֪��ʵ���͢���ȣ���ˮ��Ũ����ͬ��ʵ������Ȼ�þ��Ũ�ȸ���ʵ������Ȼ�þ��Ũ�ȡ�����ʵ������а�ɫ����������þ���ɣ��������Ԣ���һ�����ɰ�ɫ����������þ��
����NaOH��Һ��Ũ�����ٴﵽx�����������Һ����OH��Ũ��0.5x�����ڻ�Ϻ���Һ��þ����Ũ����0.014mol/L������Ҫ����������þ��������(0.5x)2��0.014��5.6��10-12�����x��4��10-5 mol/L��
�ۻ�ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ���ʽ��֪���ÿ��淴Ӧ��ƽ�ⳣ��K�� ��K��
��K�� ��Kb2/Ksp��
��Kb2/Ksp��
���㣺���鷴Ӧ���ʺ�ƽ�ⳣ���ļ��㣻���������ƽ��״̬��Ӱ�죻�ܽ�ƽ���Լ��ܶȻ������ļ����Ӧ�õ�


 ��ͼͼ�麮����ҵ������ҵ���ִ�ѧ������ϵ�д�
��ͼͼ�麮����ҵ������ҵ���ִ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���������£�2SO2(g)+O2(g)  2SO3(g) ��H<0�������й�������ȷ����
2SO3(g) ��H<0�������й�������ȷ����
| A�����{�¶ȣ�v�����v����С |
| B�����º���,����O2��O2��ת�������� |
| C�����º�ѹ������N2��ƽ�ⲻ�ƶ� |
| D�����º��ݣ�ƽ��ǰ����������ܶȱ��ֲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�ݱ�������300�桢70MPa���ɶ�����̼�������ϳ��Ҵ��ѳ�Ϊ��ʵ���䷴Ӧ�Ļ�ѧ����ʽΪ��2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) �� ����������ȷ����
CH3CH2OH(g)+3H2O(g) �� ����������ȷ����
| A����v(CO2)=2v(CH3CH2OH)ʱ����Ӧһ���ﵽƽ��״̬ |
| B����ƽ�����������ƶ�ʱ��ƽ�ⳣ��һ������ |
| C������ѹǿ�������CO2��H2��ת���� |
| D����ͬ�����£�2 mol��ԭ�������е���������1 mol����������е����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����β�������е�һ����Ӧ���£�2NO(g)+2CO(g) N2(g)+2CO2(g) ��H=��373.4kJ/mol
N2(g)+2CO2(g) ��H=��373.4kJ/mol
��Ӧ�ﵽƽ��ı�ijһ������������ʾ��ͼ���ߢ�?������ȷ����
| A���٢ޢ� | B���٢ݢ� | C���ڢۢ� | D���ۢޢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����£�������Һ�и���Ũ�ȹ�ϵ��pH�ж�����ȷ����
| A����5 mL 0.02 mol/L��H2SO4��Һ��5 mL 0.02 mol/L NaOH��Һ��ֻ�ϣ�����Ϻ���Һ�����Ϊ10 mL������Һ��pH=2 |
| B��ij���ʵ���Һ����ˮ�����c(H+) = 1��10-a mol/L����a��7����pHһ��Ϊ14��a |
| C��pH��ȵĢ�CH3COONa��C6H5ONa��NaHCO3��Һ�У�c(Na+)��С��ϵ���٣��ۣ��� |
| D��CH3COONa��Һ�м�������KNO3�����ļ�����Һһ���У� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����(t-BuNO)2���������CCl4�о����Է�����Ӧ��(t-BuNO)2 2(t-BuNO)����20��ʱ����1 L�������м���(t-BuNO)2 0.50 mol��10 minʱ��Ӧ��ƽ�⣬��ʱ(t-BuNO)2��ƽ��ת����Ϊ65%�����跴Ӧ��������Һ���ʼ��Ϊ1 L��������˵����ȷ����
2(t-BuNO)����20��ʱ����1 L�������м���(t-BuNO)2 0.50 mol��10 minʱ��Ӧ��ƽ�⣬��ʱ(t-BuNO)2��ƽ��ת����Ϊ65%�����跴Ӧ��������Һ���ʼ��Ϊ1 L��������˵����ȷ����
| A����Ӧ��ǰ10 min�ڵ�ƽ������Ϊ��(t-BuNO)=0.0325mol��L��1��min��1 |
| B�����������������䣬����ʱ������Һ�м���0.50 mol (t-BuNO)2�����´�ƽ��ʱ(t-BuNO)2�İٷֺ�����С |
| C�����������������䣬���÷�Ӧ��CCl4�н��У���ƽ�ⳣ��Ϊ1.9����(t-BuNO)2��ƽ��ת����С��65% |
| D�����������������䣬�����¶ȣ� (t-BuNO)2��ƽ��ת���ʴ���65%������������ϵ������ͼ��ʾ |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��������һ�����ȼ�ϣ���n(H2)/n(CO)=2ͨ��1L�ķ�Ӧ���У�һ�������·�����Ӧ:2CO(g)+4H2(g)  CH3OCH3(g) +H2O(g) ��H����CO��ƽ��ת�������¶ȡ�ѹǿ�仯��ϵ��ͼ��ʾ������˵����ȷ����
CH3OCH3(g) +H2O(g) ��H����CO��ƽ��ת�������¶ȡ�ѹǿ�仯��ϵ��ͼ��ʾ������˵����ȷ����
| A��������Ӧ��H>0 |
| B��ͼ��P1<P2<P3 |
| C������P3��316��ʱ�����������n(H2)=n(CH3OCH3)����ʱv(��)<v(��) |
| D������P3��316��ʱ����ʼʱn(H2)/n(CO)=3����ﵽƽ��ʱ��COת����С��50% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����Ⱥ����ܱ�������ͨ��SO2��NO2��һ��������ʹ��Ӧ�� SO2(g)+NO2(g) SO3(g)+NO(g) �ﵽƽ�⣬����Ӧ������ʱ��仯��ͼ��ʾ������ȷ�Ľ�����
SO3(g)+NO(g) �ﵽƽ�⣬����Ӧ������ʱ��仯��ͼ��ʾ������ȷ�Ľ�����
| A���淴Ӧ���ʣ�a��С�ڵ�c |
| B����Ӧ��Ũ�ȣ�a��С�ڵ�b |
| C����Ӧ��c��ʱSO2��ת������� |
| D����Ӧ�������������������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��һ���¶��£���aL�ܱ������м���1molX�����2molY���壬�������·�Ӧ��
X(g) + 2Y(g)  2Z(g) �˷�Ӧ�ﵽƽ��ı�־��
2Z(g) �˷�Ӧ�ﵽƽ��ı�־��
| A������Ӧ���淴Ӧ�����ʶ�Ϊ�� |
| B�������ڸ����ʵ�Ũ�Ȳ���ʱ��仯 |
| C��������X��Y��Z��Ũ��֮��Ϊ1��2��2 |
| D����λʱ������0.1molXͬʱ����0.2molZ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com