
| A. | 钠与水反应:Na+H2O=Na++OH-+H2↑ | |
| B. | 铝与盐酸反应:2Al+6H+=2Al3++3H2↑ | |
| C. | 氢氧化铝与盐酸反应:OH-+H+=H2O | |
| D. | 氯化铝与氨水反应:Al3++3OH-=Al(OH)3↓ |
分析 A.原子个数不守恒;
B.生成氯化铝和氢气;
C.氢氧化铝为沉淀应保留化学式;
D.一水合氨为弱电解质,应保留化学式;
解答 解:A.钠与水反应,离子方程式:2Na+2H2O=2Na++2OH-+H2↑,故A错误;
B.铝与盐酸反应,离子方程式:2Al+6H+=2Al3++3H2↑,故B正确;
C.氧化铝与盐酸反应,离子方程式:Al(OH)3+3H+=3H2O+Al3+,故C错误;
D.氯化铝与氨水反应,离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,明确反应实质,熟练掌握离子方程式书写方法即可解答,题目难度不大.


科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气通过灼热的CuO粉末 | B. | 二氧化碳通过Na2O2粉末 | ||
| C. | 铝与氧化铁高温下发生反应 | D. | 将锌粒投入FeCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质编号 | 物质转化关系 | 甲 | 乙 | 丙 | 丁 |
| ① | 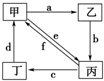 | Cu | CuO | CuCl2 | Cu(NO3)2 |
| ② | Na2CO3 | NaOH | NaHCO3 | CO2 | |
| ③ | (NH4)2SO3 | CaSO3 | SO2 | NH4HSO3 | |
| ④ | Al(OH)3 | Al2O3 | Na[Al(OH)4] | AlCl3 |
| A. | ①③ | B. | ②④ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④⑤⑦⑨ | B. | ①②⑤⑥⑧ | C. | ③④⑤⑦ | D. | ③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 次氯酸的电子式 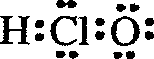 | B. | 二氧化硅分子式 SiO2 | ||
| C. | CS2结构式 S=C=S | D. | 钾离子的结构示意图如图 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com