
【题目】下列图示与对应的叙述相符的是( )
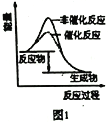


A. 图1表示分别在有、无催化剂的情况下某吸热反应过程中的能量变化
B. 图2表示常温下,等量锌粉与足量的等浓度的盐酸反应(滴加CuSO4溶液的为虚线)
C. 图3表示mg冰醋酸加水稀释过程中溶液导电能力的变化,其中醋酸的电离度c>b>a
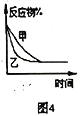
D. 图4表压强对合成氨反应的影响,乙的压强大
科目:高中化学 来源: 题型:
【题目】用下图所示装置做NaHCO3的分解实验,请回答下列问题:
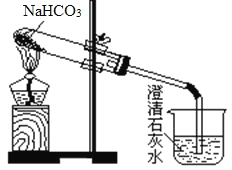
(1)试管中发生反应的化学方程式为_______。
(2)烧杯中可观察到的现象是_______。
(3)组装装置后主要实验操作有:①用酒精灯加热;②熄灭酒精灯;③检查装置的气密性;④在试管里加入NaHCO3固体;⑤将导气管撤离石灰水。则正确的操作为③→_______→_______→_______→②(填各步操作的序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了将混有Na2SO4、NH4HCO3的NaCl提纯。某学习小组设计了如图所示的方案:
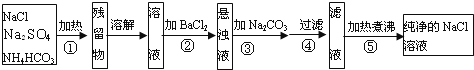
(1)操作①盛放药品的仪器名称是___________,发生反应的化学反应方程式为__________________。
(2)进行操作②后,如何判断杂质是否除尽?_______________________________________________。
(3)操作③的目的是_____________________。
(4)请你评价该设计方案设计是否严密?若不严密,请说明理由,并提出改进方案_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列仪器或装置,请回答下列问题:
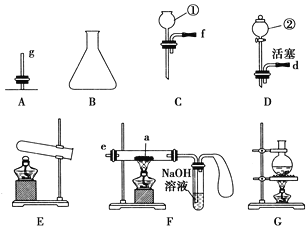
(1)仪器①的名称是________,②的名称是________。
(2)用上图仪器组装成气体发生装置:用KClO3和MnO2制O2应选的装置是________(填字母);用废H2O2与MnO2制O2,并控制产生O2的速率,应选________(填字母)。
(3)若用装置X进行“排空气法”收集制取的O2,氧气应从________(填“b”或“c”)端导入。若瓶中装满水,用排水法收集氧气,氧气应从________(填“b”或“c”)端导入。
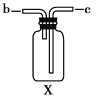
(4)若用F装置进行CO还原Fe2O3的实验,实验室制取CO的方法一般采取甲酸脱水法(HCOOH![]() CO↑+H2O),用纯净的CO完成该实验。
CO↑+H2O),用纯净的CO完成该实验。
①除F、X外还需要的装置有________,X中应加入的试剂是________,X与其它导管连接的顺序是________(填导管口的序号);
②实验时,a处的可能的现象为_________________;F装置中气球的作用是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2,装置如下图所示。
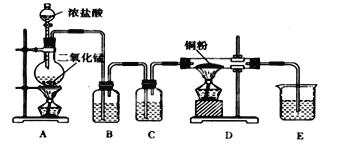
(1)B中选用的试剂是____________,其作用是__________;C中选用的试剂的作用是_________
(2)D中反应的化学方程式是_______________________
(3)某学生应用如图所示的方法研究物质的性质,其中气体X的主要成分是氯气。回答下列问题:
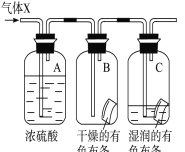
① 与研究目的直接相关的B、C中的实验现象是________。
② 如果通入气体中混有SO2,能否看到相同的现象? _________(填“能”、“不能”或者“”“不能确定”),用化学方程式进行解释: ______________________
③从物质性质的方面来看,这样的实验设计还存在事故隐患,事故表现是最后缺少一个____________装置,用化学方程式解释其原理__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,22.4LN2和H2混合气中含2NA 个原子
B. 78gNa2O2与足量的CO2完全反应,转移的电子数为2NA
C. 1 L1 mol·L-1NH4Cl溶液中,NH4+的数量为NA
D. 室温下, pH=13的NaOH 溶液中,则溶液中 OH- 离子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某试剂瓶上贴有如下标签,对该试剂理解正确的是
![]()
A. 该溶液中含有的微粒主要有:NaCl、Na+、Cl-、H2O
B. 若取50毫升溶液,其中的c(Cl-)=0.05 mol/L
C. 若取该溶液与0.1 mol/L AgNO3 100 mL溶液完全反应,需要取该溶液10 mL
D. 该溶液与1.0mol/LNa2SO4溶液的c(Na+)相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.由Na2CO3 + SiO2 ![]() Na2SiO3 + CO2↑可知,酸性H2SiO3>H2CO3
Na2SiO3 + CO2↑可知,酸性H2SiO3>H2CO3
B.氢氟酸需要密封存放在橡胶塞的玻璃试剂瓶中
C.向硅酸钠溶液中加入盐酸产生白色沉淀,过量时沉淀溶解
D.瓷坩埚、氧化铝坩埚均不可作为融化NaOH固体的装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向。
(1)CO2的电子式是 ,所含化学键的类型是 。
(2)工业上用CO2和H2反应合成二甲醚。已知:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.1 kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.1 kJ·mol-1
2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
①写出CO2(g)和H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式 。
②一定条件下,上述合成二甲醚的的反应达到平衡状态后,若改变反应的某个条件,下列变化能说明平衡一定向正反应方向移动的是(只有一个选项符合题意) (填字母代号)。
a.逆反应速率先增大后减小
b.H2的转化率增大
c.CO2的体积百分含量减小
d.容器中c(H2)/c(CO2)的值减小
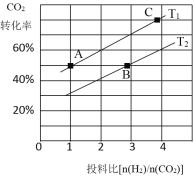
③在某压强下,合成二甲醚的反应在不同温度、不同投料比时,CO2的平衡转化率如右图所示。T1温度下,将6 molCO2和12 molH2充入2 L的密闭容器中,5 min后反应达到平衡状态,则0~5 min内的平均反应速率v(CH3OCH3)= ;KA、KB 、KC三者之间的大小关系为 。
(3)CO2溶于水形成H2CO3。已知常温下H2CO3的电离平衡常数K1=4.4×10-7,K2=4.7×10-11,NH3·H2O的电离平衡常数K=1.75×10-5。常温下,用氨水吸收CO2可得到NH4HCO3溶液,NH4HCO3溶液显 ;(填“酸性”、“中性”或“碱性”);请计算反应NH4++HCO3-+H2O![]() NH3·H2O+H2CO3的平衡常数K= 。
NH3·H2O+H2CO3的平衡常数K= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com