
【题目】下列说法不正确的是( )
A.在CH3COOH分子中的所有碳原子和氧原子都在同一平面
B.在 中单体为
中单体为![]() 和NC-CHO
和NC-CHO
C.1mol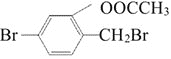 与NaOH溶液完全反应,消耗NaOH5mol
与NaOH溶液完全反应,消耗NaOH5mol
D.![]() 与Br21︰1加成可有4种加成产物
与Br21︰1加成可有4种加成产物
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】用50mL![]() 盐酸跟50mL
盐酸跟50mL![]() NaOH溶液中和反应过程中所放出的热量计算中和热。
NaOH溶液中和反应过程中所放出的热量计算中和热。
(1)烧杯间填满泡沫塑料的作用是______;
(2)大烧杯上若不盖硬纸板,求得的中和热数值______![]() 填“偏大”、“偏小”、“无影响”
填“偏大”、“偏小”、“无影响”![]()
(3)如图所示,仪器A的名称是______;

(4)重复三次实验,记录的实验数据如下:
实验用品 | 溶液温度 | |||
|
| |||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
已知:![]() ,反应后溶液的比热容c为
,反应后溶液的比热容c为![]() ,各物质的密度均为
,各物质的密度均为![]() 。计算
。计算![]() ______
______![]()
(5)实验中改用80mL![]() 盐酸跟100mL
盐酸跟100mL![]() NaOH溶液进行反应,与上述实验相比,所放出的热量______
NaOH溶液进行反应,与上述实验相比,所放出的热量______![]() 填“相等、“不相等”
填“相等、“不相等”![]() ,所求中和热______
,所求中和热______![]() 填“相等、“不相等”
填“相等、“不相等”![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中第ⅦA 族元素的单质及其化合物的用途广泛。
(1)能作为氯、溴、碘元素非金属性递变规律的判断依据是_______(填序号)
a.Cl2、Br2、I2 的熔点 b.Cl2、Br2、I2 的氧化性
c.HCl、HBr、HI 的热稳定性 d.HCl、HBr、HI 的酸性
(2)工业上,通过如下转化可制得 KClO3 晶体:
NaCl溶液![]() NaClO3
NaClO3![]() KClO3晶体
KClO3晶体
①完成 I 中反应的总化学方程式:_______NaCl+________H2O =_______NaClO3+_______。
②反应Ⅰ中 NaClO3 是_______极(选填“阴”或“阳”极)产物。
③Ⅱ中转化的基本反应类型是_________,该反应过程能析出 KClO3 晶体而无其它晶体析出的原因是_______。
(3)一定条件,在水溶液中 1 mol Cl-、ClOX-(x=1,2,3,4)的能量(kJ)相对大小如图所示。
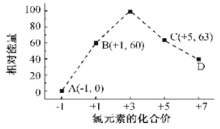
①D 是_______(填离子符号)。
②B→A+C 反应的离子方程式为_______;生成 1mol C 时,________(填吸收或放热)________kJ 的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某药物中间体的合成路线如下![]() 下列说法正确的是()
下列说法正确的是()
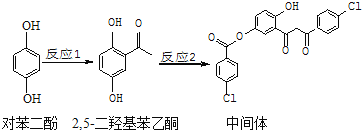
A.对苯二酚在空气中能稳定存在
B.1mol该中间体最多可与11![]() 反应
反应
C.2,![]() 二羟基苯乙酮能发生加成、取代、缩聚反应
二羟基苯乙酮能发生加成、取代、缩聚反应
D.该中间体分子中含有1个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用有机含碘![]() 主要以
主要以![]() 和
和![]() 的形式存在
的形式存在![]() 废水制备单质碘的实验流程如下:
废水制备单质碘的实验流程如下:
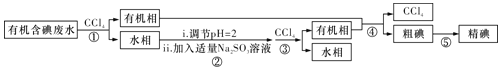
已知:Ⅰ![]() 碘的熔点为
碘的熔点为![]() ,但固态的碘可以不经过熔化直接升华;
,但固态的碘可以不经过熔化直接升华;
Ⅱ![]() 粗碘中含有少量的
粗碘中含有少量的![]() 杂质。
杂质。
下列说法正确的是( )
A.操作![]() 中发生反应的离子方程式为
中发生反应的离子方程式为![]()
B.操作![]() 和
和![]() 中的有机相从分液漏斗上端倒出
中的有机相从分液漏斗上端倒出
C.操作![]() 为过滤
为过滤
D.操作![]() 可用如图所示的水浴装置进行
可用如图所示的水浴装置进行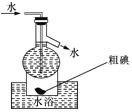
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应在生产、生活中应用广泛,酸性KMnO4、H2O2、Fe(NO3)3是重要的氧化剂.已知在酸性条件下,KMnO4被还原为Mn2+。用所学知识回答问题:
(1)3H2SO4+2KMnO4+5H2O2=K2SO4+2MnSO4+5O2↑+8H2O,当有6mol H2SO4参加反应的过程中,有___mol还原剂被氧化。
(2)在稀硫酸中,KMnO4能将H2C2O4氧化为CO2。该反应的离子方程式为___。
(3)取300mL2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成KIO3,则消耗KMnO4的物质的量的是___mol。
(4)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是___,又变为棕黄色的原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】J、L、M、R、T 是原子序数依次增大的短周期主族元素,J、R 在周期表中的相对位置如表; J 原子最外层电子数是其内层电子数的 2 倍;L 的最简单气态氢化物甲的水溶液显碱性;M 是地壳中含量最多的金属元素。

(1)M 的离子结构示意图为_______;元素 T 在周期表中位于第________周期第_______族。
(2)J 元素是_________(用元素符号表示);J 和氢组成的 10 电子化合物的化学式为_________。
(3)M 和 T 形成的化合物属于_______(填“离子化合物”、或“共价化合物”),其中所有原 子都满足最外层 8 电子结构的分子是_______(填化学式),电子式为_______。
(4)元素 M 形成的简单离子的水溶液与甲的水溶液反应的离子方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容密闭容器中,当物质的下列物理量不再变化时,不能表明反应:![]() 已达平衡的是( )
已达平衡的是( )
A.混合气体的密度B.混合气体的压强
C.![]() 的物质的量浓度D.混合气体的平均相对分子质量
的物质的量浓度D.混合气体的平均相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是几种常见有机物之间的转化关系图。C具有果香味。
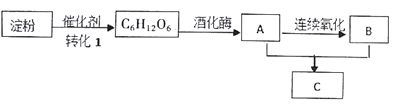
根据以上信息及各物质的转化关系完成下列各题:
(1)A的结构简式为_______,工业上用乙烯生产A的化学方程式为__________。
(2)B物质的俗称为_____,B可与纯碱溶液反应,写出该反应方程式_____________。
(3)A+B→C的化学方程式为__________,反应类型为_________反应。
(4)下列说法正确的是_______。
a.上述有机物中只有C6H12O6属于糖类物质
b.物质A和B都属于电解质
c.物质C和油脂类物质互为同系物
d.转化1可在人体内完成,该催化剂属于蛋白质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com