
| A. | 2015年诺贝尔化学奖颁给了研究细胞修复自身DNA机制的三位科学家.DNA属于有机高分子,化学家鲍林(L.Pauling)提出的氢键理论和蛋白质分子的螺旋结构模型,为DNA分子双螺旋结构模型的提出奠定了基础 | |
| B. | 生物炼铜是指铜矿石在细菌作用下可把不溶性的硫化铜转化为可溶性铜盐,使铜的冶炼变得简单 | |
| C. | 埃博拉病毒对化学药品敏感,乙醇、次氯酸钠溶液、双氧水均可以将病毒氧化而达到消毒的目的 | |
| D. | 扫描隧道显微技术、超分辨荧光显微技术等的发展促进了人类对微观结构的探索,可实现对原子或分子的操控,使科学研究迈入更高的水平层次 |
分析 A、化学家鲍林提出了氢键理论和蛋白质分子的螺旋结构模型;
B、微生物法是采用某些细菌能用空气中的氧气氧化硫化铜矿石;
C、乙醇使蛋白质变性;
D、新科技的发展促进人们的研究能力和水平.
解答 解:A、化学家鲍林提出了氢键理论和蛋白质分子的螺旋结构模型,为DNA分子双螺旋结构模型的提出奠定了基础,故A正确;
B、把不溶性的硫化铜氧化,硫从负二价被氧化成正六价,故最后转化成可溶的硫酸铜,故B正确;
C、乙醇消毒液消毒是因为可以使蛋白质变性,而并非是将病毒氧化,而次氯酸钠溶液可以将病毒氧化而达到消毒的目的,故C错误;
D、扫描隧道显微技术、超分辨率荧光显微技术等技术的发展促进了人类对物质微观结构的探索,使科学研究迈入更高水平层次,故D正确.
故选C.
点评 本题考查了化学史、前沿科技的理解,注意对相关知识的积累,侧重于考查学生对基础知识的应用能力.


科目:高中化学 来源: 题型:解答题
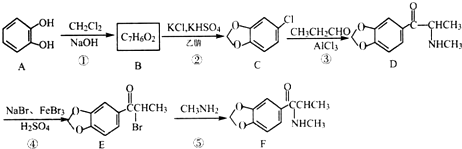
 .
. (填结构简式).
(填结构简式).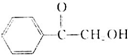 )的合成路线.
)的合成路线.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
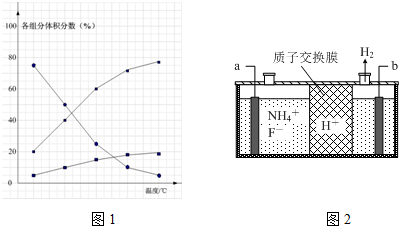
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 容量瓶、量筒和滴定管上都标有使用温度,容量瓶无“0”刻度,量筒、滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 | |
| B. | 向3支试管中各加入2mL 0.1mol•L-1酸性高锰酸钾溶液和2mL 0.01mol•L-1 H2C2O4溶液,将它们分别置于冰水、室温下、80℃热水中,观察比较褪色快慢 | |
| C. | 皂化反应结束后的混合液中加入饱和食盐水,再通过分液操作分离出硬脂酸钠 | |
| D. | 为保证实验安全,金属钠切割下来的表层物质应放回原试剂瓶,不能在研钵中研磨氯酸钾或硝酸钾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自然界中植物通过光合作用将太阳能转化为生物质能,而农村沼气池的建造、农作物制乙醇,都是有效的利用生物质能 | |
| B. | 纳米TiO2光触媒技术制成的“木地板精油”能将水气转化为活性氧,可以有效降解甲醛、苯、氨等居室污染物 | |
| C. | 高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强酸、强碱都会“断路” | |
| D. | 同位素在医学显像、诊断和治疗,以及在改进农产品质量、增加产量等技术方面应用广泛 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
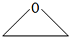 .
.
 ;
;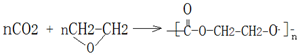 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若反应①中生成3.36 L氢气,则一定有2.7 g铝生成 | |
| B. | 氢化锂也是一种储氢材料,供氢原理为LiH+H2O═LiOH+H2↑ | |
| C. | 生成等质量的氢气,反应①、②转移电子数之比为4:3 | |
| D. | LiAlH4是共价化合物,LiH是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液中:c(H+)+c(H2CO3)=2c(CO32-)+c(OH-) | |
| B. | 向0.1 mol•L-1的NH4Cl溶液中通入一定量的NH3后:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| C. | 向CH3COOH溶液中滴加NaOH使pH>7溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 0.3 mol•L-1的 HY溶液与0.3 mol•L-1的NaOH溶液等体积混合后所得pH=9的溶液中:c(OH-)-c(HY)=c(H+)=1×10-9 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
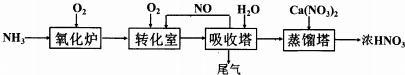
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com