
关于化学平衡常数、电离平衡常数、水的离子积常数和溶解平衡常数,下列说法正确的是
A.四种平衡常数都是一个比值,没有单位
B.四种平衡常数都是温度的函数,温度升高其值都增大
C.一个化学反应的平衡常数与物质的计量数无关
D.对于同类型反应,化学平衡常数K的大小反映了化学反应可能进行的程度
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2013-2014四川省下学期期中考试高一化学试卷(解析版) 题型:填空题
(8分)被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.下图为氢氧燃料电池的结构示意图,
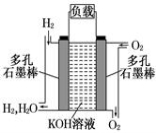
电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:
(1) 写出氢氧燃料电池工作时正极电极反应方程式: ___________ 。
(2)如果该氢氧燃料电池每转移0.1mol电子,消耗标准状况下___________L氧气。
(3) 若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为___________________。 电池总离子反应方程式为_______________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省资阳市高一下学期期末考试化学试卷(解析版) 题型:选择题
对于锌、铜和稀硫酸组成的原电池(如下图),下列有关说法错误的是

A.溶液中H+向负极移动 B.电子由Zn经外电路流向Cu
C.Zn电极反应:Zn-2e-=Zn2+D.Cu是正极
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省资阳市二下学期期末考试化学试卷(解析版) 题型:实验题
(8分)下图为苯和溴的取代反应的实验装置图,其中A为由具有支管的试管制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑粉。
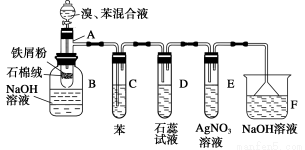
填写下列空白:
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中所发生有机反应的化学方程式:____________________________________________________________
(2)试管C中苯的作用是 。反应开始后,观察D和E两试管,看到的现象为 。
(3)反应2~3 min后,在B中的NaOH溶液里可观察到的现象是
。
(4)在上述整套装置中,具有防倒吸作用的仪器有(填字母): 。
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省资阳市二下学期期末考试化学试卷(解析版) 题型:选择题
观察下列几个装置示意图,有关叙述正确的是

A.装置①中阳极上析出红色固体
B.装置②的待镀铁制品应与电源负极相连
C.装置③中外电路电子由b极流向a极
D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省资阳市二下学期期末考试化学试卷(解析版) 题型:选择题
下列事实与电化学腐蚀无关的是
A.生铁比纯铁易生锈
B.黄铜(铜锌合金)制品不易产生铜绿
C.纯银饰品久置表面变暗
D.与铜管连接的铁管易生锈
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省资阳市二下学期期末考试化学试卷(解析版) 题型:选择题
“绿色化学”要求化学反应尽可能不产生“副产物”,下列反应最符合“绿色化学”要求的是
A.苯乙烯在一定条件下制聚苯乙烯B.乙醇与浓硫酸共热制乙烯
C.乙醇催化氧化制乙醛 D.乙烷与氯气反应制氯乙烷
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省眉山市高三第二次诊断性考试理综化学试卷(解析版) 题型:选择题
为减小CO2对环境的影响,在倡导“低碳”的同时,还需加强对CO2创新利用的研究。已知:CO2(g)+3H2(g) 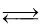 CH3OH(g)+H2O(g) △H=-49.0 kJ/mol。T1℃时,向体积为1L的恒容密闭容器中充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示,且平衡时体系压强为P1。下列叙述中不正确的是
CH3OH(g)+H2O(g) △H=-49.0 kJ/mol。T1℃时,向体积为1L的恒容密闭容器中充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示,且平衡时体系压强为P1。下列叙述中不正确的是
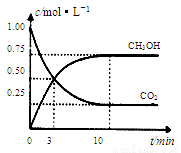
A.0~3 min内,v(CO2)正 =v (CH3OH)正
B.其他条件不变,若向平衡后的体系中充入1mol氦气,体系压强增大平衡将向正方向移动
C.在T1℃时,若起始时向容器中充入2molCO2和6mol H2 , 测得平衡时容器内压强为P2, 则 P2<2P1
D.T2℃时,上述反应平衡常数为4.2,则T2>T1
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省成都市高三第三次诊断性考试理综化学试卷(解析版) 题型:选择题
常温下,下列指定条件下能大量共存的微粒是
A、乙醇稀溶液:K+、Na+、SO42—、OH—
B、氨水溶液:Mg2+、Ag+、NO3—、CH3COOH
C、c(OH—)/c(H+)=1012溶液:H2S、Ca2+、Ba2+、HCO3—
D、使石蕊变红的溶液:Fe2+、Al3+、ClO—、CO32—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com