
 可简化为
可简化为 杀虫剂“阿乐丹”的结构表示为
杀虫剂“阿乐丹”的结构表示为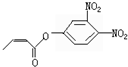 ,若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )
,若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )| A. | 均能发生银镜反应 | B. | 遇FeCl3溶液均显紫色 | ||
| C. | 均能与NaHCO3溶液发生反应 | D. | 均能与浓溴水发生反应 |
分析 有机物含有酯基,可发生水解反应,含有碳碳双键,可发生加成、氧化和加聚反应,水解产物为CH3CH=CHCOOH,另一种产物为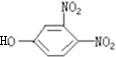 ,含有酚羟基和硝基,酚羟基可发生取代、氧化和显色反应,以此解答该题.
,含有酚羟基和硝基,酚羟基可发生取代、氧化和显色反应,以此解答该题.
解答 解:水解产物为CH3CH=CHCOOH和 ,
,
A.均不含-CHO,不能发生银镜反应,故A错误;
B.只有 含酚羟基,遇FeCl3溶液显紫色,故B错误;
含酚羟基,遇FeCl3溶液显紫色,故B错误;
C.CH3CH=CHCOOH含有羧基,与NaHCO3溶液反应,而 含有酚羟基,与NaHCO3溶液不反应,故C错误;
含有酚羟基,与NaHCO3溶液不反应,故C错误;
D.CH3CH=CHCOOH含有碳碳双键,可与溴水发生加成反应, 含有酚羟基,可与溴水发生取代反应,故D正确.
含有酚羟基,可与溴水发生取代反应,故D正确.
故选D.
点评 本题综合考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的官能团的性质,为解答该题的关键,难度不大,注意相关基础知识的积累.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 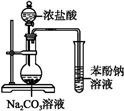 证明酸性:盐酸>碳酸>苯酚 | B. |  实验室制取乙酸乙酯 | ||
| C. |  石油分馏 | D. |  实验室制取硝基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
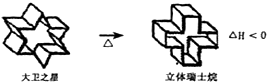
| A. | 立体瑞土烷的分子式为C24H26 | |
| B. | 大卫之星烷与立体瑞士烷的一氯代物均只有一种 | |
| C. | 大卫之星烷比立体瑞士烷更稳定 | |
| D. | 大卫之星烷与立体瑞士烷互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu→Cu(NO3)2 | B. | C→CO2 | C. | CuO→Cu(NO3)2 | D. | Fe2O3→Fe(NO3)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2,3-二甲基丁烷和2-甲基丁烷 | B. | 戊烷和环己烷 | ||
| C. | 丙烷和2-甲基丙烷 | D. | 2,3-二甲基丁烷和和己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com