
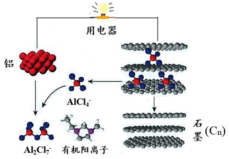
 近期,科学家成功研制出一种可在一分钟内完成充放电的超常性能铝离子电池.该电池内部的A1Cl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
近期,科学家成功研制出一种可在一分钟内完成充放电的超常性能铝离子电池.该电池内部的A1Cl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )| A. | 放电时,铝为负极、石墨为正极 | |
| B. | 充电时,A1Cl4-向石墨电极移动 | |
| C. | 放电时,负极的电极反应式为A1十7A1Cl4--3e-=4 A12Cl7- | |
| D. | 充电时,电子从石墨电极直接经导线流入铝电极,然后再经电解质溶液流回石墨电极 |
分析 由示意图可知放电时铝为负极,被氧化生成Al2Cl7-,电极方程式为Al+7AlCl4--3e-═4Al2Cl7-,正极反应为3Cn[AlCl4]+3e-=3Cn+3AlCl4-,电解时阳极发生氧化反应,电解方程式为Cn+AlCl4--e-═Cn[AlCl4],阴极发生还原反应,电极方程式为4Al2Cl7-+3e-=Al+7AlCl4-,以此解答该题.
解答 解:A.放电时,铝是活泼的金属铝是负极,不活泼石墨为正极,故A正确;
B.电解时阳极发生氧化反应,电解方程式为Cn+AlCl4--e-═Cn[AlCl4],所以充电时,A1Cl4-向石墨电极移动,故B正确;
C.放电时负极发生氧化反应生成铝离子,铝离子与AlCl4-结合生成Al2Cl7-,所以电极反应式为:Al-3e-+7AlCl4-═4Al2Cl7-,故C正确;
D.充电时,负极与外接电源的负极相连,正极与外接电源的正极相连,电子不能通过电解质溶液,故D错误;
故选D.
点评 本题考查学生二次电池的工作原理以及原电池和电解池的工作原理知识,为高频考点,侧重学生的分析能力的考查,属于综合知识的考查,难度中等,注意把握电极的判断方法和电极方程式的书写.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 元素的非金属性次序为c>b>a | |
| B. | a-的还原性弱于c-的还原性 | |
| C. | d和其他3种元素均能形成离子化合物 | |
| D. | 元素a、b、c各自最高和最低化合价的代数和分别为0、4、6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酶属于碳水化合物,是生物体中重要的催化剂 | |
| B. | 纤维素为天然高分子化合物,遇碘水会变蓝色 | |
| C. | 某些卤代烃能破坏臭氧层,使卤代烃的使用受到限制 | |
| D. | 某有机物的1H核磁共振谱图中特征峰的数目就是氢原子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作 | 现象 | 结论 | |
| A | 先加硝酸,再滴加BaCl2溶液 | 产生白色沉淀 | 原溶液中一定有SO42- |
| B | 先加入H2O2溶液,再加KSCN溶液 | 溶液呈血红色 | 原溶液中一定有Fe2+ |
| C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中一定有Na+、无K+ |
| D | 滴加NaOH溶液,加热,将湿润红色石蕊试纸置于试管口 | 试纸变蓝 | 原溶液中一定有NH4+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O的电子式: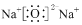 | B. | F-的结构示意图: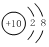 | ||
| C. | 中子数为20的Ar原子:${\;}_{18}^{20}$Al | D. | 苯甲酸的结构简式: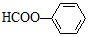 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该装置的能量转化方式为太阳能转化为电能 | |
| B. | 工作时,阳极附近pH减小 | |
| C. | 电路中每转移4mol电子,捕获44g二氧化碳 | |
| D. | 阴极的电极反应为CO2+2e-=CO+O2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类、油脂、蛋白质都能发生水解反应 | |
| B. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| C. | 苯不能使溴的四氯化碳溶液褪色,但能与H2发生加成反应 | |
| D. | 因分子中均含有官能团“-OH”,故乙醇、乙酸水溶液均呈酸性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com