
| A. | CH4 C2H4 | B. | CH4 C3H4 | C. | C2H4 C3H4 | D. | C2H2 C3H6 |
分析 设有机物的平均式为CxHy,燃烧通式为:CxHy+(x+$\frac{y}{4}$)O2→xCO2+$\frac{y}{2}$H2O,105℃时生成的水为气体,反应前后气体体积不变,则1+x+$\frac{y}{4}$=x+$\frac{y}{2}$,解答y=4,即混合气中平均含有H原子数为4,由于是任意比混合,故各组分分子中H原子数目均为4.
解答 解:设有机物的平均式为CxHy,则有CxHy+(x+$\frac{y}{4}$)O2→xCO2+$\frac{y}{2}$H2O,105℃时生成的水为气体,有机物燃烧前后体积不变,则1+x+$\frac{y}{4}$=x+$\frac{y}{2}$,解答y=4,即混合气中平均含有H原子数为4,由于是任意比混合,故各组分分子中H原子数目均为4.
A.CH4、C2H4中H原子数都为4,符合题意,故A不选;
B.CH4、C3H4中H原子数都为4,符合题意,故B不选;
C.C2H4、C3H4中H原子数都为4,符合题意,故C不选;
D.C2H2、C3H6按物质的量1:1混合时平均H原子数目为4,不符合任意比,故D选
故选:D.
点评 本题考查有机物的确定,题目难度中等,注意利用烃燃烧通式、平均值法计算解答,有利于培养学生的分析理解能力及化学计算能力.


 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:选择题
| A. | NH4+、Mg2+、SO42-、Cl- | B. | Fe3+、K+、Cl-、NO3- | ||
| C. | K+、Ba2+、NO3-、SO42- | D. | Na+、NH4+、Cl-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
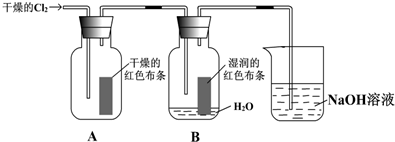
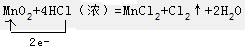
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
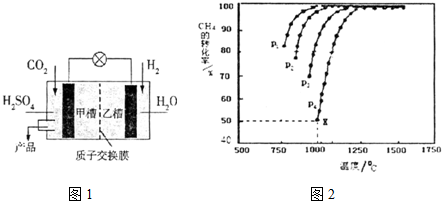 第21届联合国气候大会于2015年11月30日在巴黎召开,会议的主题是减 少温室气体排放量.
第21届联合国气候大会于2015年11月30日在巴黎召开,会议的主题是减 少温室气体排放量.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入NaOH溶液,生成灰白色沉淀迅速变成灰绿色,最后变成红褐色 | |
| B. | 加入NaOH溶液,生成红褐色沉淀 | |
| C. | 加入硫氰化钾溶液,显示红色 | |
| D. | 加入氨水,生成红褐色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- | |
| B. | 0.1mol•L-1的NaOH溶液:K+、Na+、SO42-、CO32- | |
| C. | 0.1mol•L-1FeCl3溶液:K+、NH4+、SO42-、SCN- | |
| D. | 使紫色石蕊试液变红的溶液:Ca2+、Na+、ClO-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com