
某浓度的氨水中存在下列平衡:NH3•H2O⇌NH4++OH﹣,如想增大NH4+的浓度,而不增大OH﹣的浓度,应采取的措施是( )
|
| A. | 适当升高温度 | B. | 加入NaOH固体 |
|
| C. | 通入NH3 | D. | 加入NH4Cl固体 |
| 弱电解质在水溶液中的电离平衡. | |
| 专题: | 电离平衡与溶液的pH专题. |
| 分析: | 增大铵根离子浓度而不增大氢氧根离子浓度,说明应该加入含有铵根离子的物质,据此分析解答. |
| 解答: | 解:A.升高温度促进一水合氨电离,则溶液中铵根离子和氢氧根离子浓度都增大,所以不符合题意,故A错误; B.加入NaOH固体,溶液中氢氧根离子浓度增大,抑制一水合氨电离,则铵根离子浓度减小,故B错误; C.通入氨气,溶液中一水合氨浓度增大,一水合氨电离出的氢氧根离子和铵根离子浓度都增大,故C错误; D.加入氯化铵,铵根离子浓度增大,抑制一水合氨电离,则氢氧根离子浓度减小,符合题意,故D正确; 故选D. |
| 点评: | 本题考查了弱电解质的电离,明确弱电解质电离的影响因素是解本题关键,再结合题意分析解答,题目难度不大. |


科目:高中化学 来源: 题型:
实验室需配制一种仅含四种离子(不包括水电离出的离子)的无色混合溶液,且在混合溶液中四种离子的物质的量浓度均为1 mol·L-1。下面四个选项中能达到此目的的是( )
A.Na+、K+、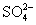 、Cl-
、Cl-
B.Cu2+、K+、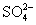 、
、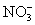
C.H+、K+、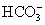 、Cl-
、Cl-
D.Mg2+、Na+、Cl-、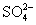
查看答案和解析>>
科目:高中化学 来源: 题型:
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
2NH3(g)+NO(g)+NO2(g)⇌2N2(g)+3H2O(g)△H<0,在恒容的密闭容器中,下列有关说法正确的是( )
|
| A. | 平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
|
| B. | 单位时间内消耗NO和N2的物质的量比为1:2时,反应达到平衡 |
|
| C. | 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
|
| D. | 平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液可能含有Cl﹣、SO42﹣、CO32﹣、NH4+、Fe3+、Al3+和K+.取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.由此可知原溶液中( )
A.至少存在5种离子
B.Cl﹣一定存在,且c(Cl‑)≥0.4mol/L
C.SO42﹣、NH4+、一定存在,Cl﹣可能不存在
D.CO32﹣、Al3+一定不存在,K+可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
碳及其化合物有广泛的用途。
(1)反应C(s)+ H2O(g) 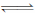 CO(g) +H2(g);ΔH= +131.3 kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
CO(g) +H2(g);ΔH= +131.3 kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
A.增加碳的用量
B.升高温度
C.用CO吸收剂除去CO
D.加入催化剂
(2)已知,C(s)+ CO2(g)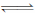 2CO(g);ΔH=+172.5kJ•mol-1,则反应 CO(g)+H2O(g)
2CO(g);ΔH=+172.5kJ•mol-1,则反应 CO(g)+H2O(g)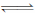 CO2(g)+H2(g)的ΔH= kJ•mol-1。
CO2(g)+H2(g)的ΔH= kJ•mol-1。
(3)CO与H2一定条件下反应生成甲醇(CH3OH),甲醇是一种燃料,可利用甲醇设计一个燃料电池,用稀硫酸作电解质溶液,多孔石墨做电极,该电池负极反应式为 。
(4)在一定温度下,将CO(g)和H2O(g)各0.16 mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g)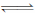 CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
| t/min | 2 | 4 | 7 | 9 |
| n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
①其他条件不变,降低温度,达到新平衡前v(逆)_____v(正)(填“>”、“<”或“=”)。
②该温度下,此反应的平衡常数K= 。
③其他条件不变,再充入0.1mol CO和0.1mol H2O(g),平衡时CO的体积分数 (填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B的混合气体在密闭容器中发生如下反应:xA(g)+yB(g)═zC(g)△H<0.达到化学平衡后测得A的浓度为0.5mol•L﹣1;保持温度不变,将密闭容器的容积缩小至原来的一半,再次达到平衡时,测得A的浓度为0.9mol•L﹣1.则下列有关判断正确的是( )
|
| A. | 平衡向正反应方向移动了 | B. | x+y<z |
|
| C. | B的转化率下降 | D. | C的体积分数减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对化学平衡移动的分析中,不正确的是( )
①已达平衡的反应C(s)+H2O(g)⇌CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
②已达平衡的反应N2(g)+3H2(g)⇌2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体体积减小的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动.
|
| A. | ①④ | B. | ①②③ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
将①H+ ②Cl- ③Al3+ ④K+ ⑤S2- ⑥OH- ⑦NO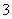 ⑧NH
⑧NH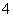 分别加入H2O中,基本上不影响水的电离平衡的是( )
分别加入H2O中,基本上不影响水的电离平衡的是( )
A.①③⑤⑦⑧ B.②④⑦
C.①⑥ D.②④⑥⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com