
|
(创新)在恒容的密闭容器中充入2 mol A和1 mol B,反应2A(g)+B(g) | |
| [ ] | |
A. |
1 |
B. |
2 |
C. |
3 |
D. |
4 |
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
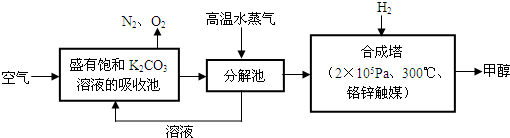
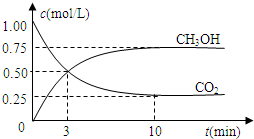
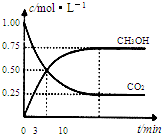 为减小CO2对环境的影响,在倡导“低碳”的同时,还需加强对CO2创新利用的研究.已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.T1℃时,向体积为1L的恒容密闭容器中充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示,且平衡时体系压强为P1.下列叙述中不正确的是( )
为减小CO2对环境的影响,在倡导“低碳”的同时,还需加强对CO2创新利用的研究.已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.T1℃时,向体积为1L的恒容密闭容器中充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示,且平衡时体系压强为P1.下列叙述中不正确的是( )| A、0~3min内,v(CO2)正=v (CH3OH)正 | B、其他条件不变,若向平衡后的体系中充入1mol氦气,体系压强增大平衡将向正方向移动 | C、在T1℃时,若起始时向容器中充入2molCO2和6mol H2,测得平衡时容器内压强为P2,则 P2<2P1 | D、T2℃时,上述反应平衡常数为4.2,则T2>T1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com