
| A. | Fe2O3常用作红色油漆和涂料 | B. | 碳酸氢钠可用于治疗胃酸过多 | ||
| C. | 二氧化硅可用于制造集成电路 | D. | Cl2可用于制漂白粉 |
分析 A.Fe2O3为红色物质,难溶于水;
B.胃酸主要成分是盐酸,碳酸氢钠腐蚀性较小,和盐酸反应;
C.二氧化硅为绝缘体,是光导纤维的成分,集成电路利用的是单质硅的性质;
D.氯气和氢氧化钙之间反应可以得到漂白粉,
解答 解:A.Fe2O3为红色物质,不溶于水则常用作红色油漆和涂料,故A正确;
B.胃酸主要成分是盐酸,所以碳酸氢钠可用于治疗胃酸过多的反应物是碳酸氢钠和盐酸,生成物是氯化钠、水、二氧化碳,方程式是:NaHCO3+HCl═NaCl+H2O+CO2↑,故B正确;
C.二氧化硅为绝缘体,不导电,晶体硅是良好的半导体材料可用于制造集成电路,故C错误;
D.工业上将Cl2通入石灰乳制取漂白粉,反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.故D正确;
故选C.
点评 本题考查了物质性质和应用,主要是铁、钠、硅、氯及其化合物性质,注意知识积累,题目较简单.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:解答题
| 实验编号 | 反应物 | 加入物质 |
| ① | 10mL 2% H2O2溶液 | 无 |
| ② | 10mL 5% H2O2溶液 | 无 |
| ③ | 9mL 5% H2O2溶液 | 1mL 水 |
| ④ | 9mL 5% H2O2溶液 | 1mL 0.1mol•L-1 HCl溶液 |
| ⑤ | 9mL 5% H2O2溶液 | 1mL 0.1mol•L-1 NaOH溶液 |

| 物理量 实验序号 | V[30% H2O2]/mL | … | |
| 1 | a | … | |
| 2 | a | … |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
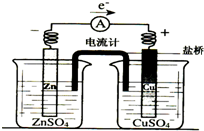
| A. | 铜片上有气泡逸出 | |
| B. | 取出盐桥后,电流计依然发生偏转 | |
| C. | 反应中,盐桥中的K+会移向CuSO4溶液 | |
| D. | 铜片上发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ②③ | D. | ③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 王水能溶解黄金,但不能溶解白金 | |
| B. | HAuCl4具有很强的氧化性 | |
| C. | 盐酸有很强的还原性 | |
| D. | 浓盐酸和浓硝酸按照体积比1:3能配成王水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
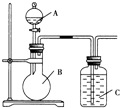 某甲同学设计如图装置,比较非金属元素的非金属性强弱.请按要求回答下列问题:
某甲同学设计如图装置,比较非金属元素的非金属性强弱.请按要求回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2═CH-CH═CH2 1,3-二丁烯 | B. | CH3-CH2-CH═CH2 3-丁烯 | ||
| C. | 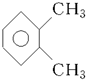 对二甲苯 对二甲苯 | D. | 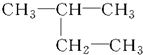 3-甲基丁烷 3-甲基丁烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com