
【题目】回答下列问题:
(1)有一种溶液除H+、OH-外,还有Na+、SO![]() 和Cl-,测得三种离子的浓度分别是0.01 mol·L-1、0.0035 mol·L-1和0.004 mol·L-1,该溶液的pH为________。
和Cl-,测得三种离子的浓度分别是0.01 mol·L-1、0.0035 mol·L-1和0.004 mol·L-1,该溶液的pH为________。
(2)NH4Cl溶液显酸性,试用离子方程式表示这一原理______________________。
(3)液氨的电离类似于水,试写出液氨的电离方程式________________________________ ;在液氨中加入NH4Cl,平衡将向________移动。
【答案】3 H2O+![]() NH3·H2O+H+ 2NH3
NH3·H2O+H+ 2NH3![]() +
+![]() 逆反应方向
逆反应方向
【解析】
(1) Na+、SO42-和Cl-三种离子的浓度分别是0.01 mol·L-1、0.0035 mol·L-1和0.004 mol·L-1,溶液中的阴离子所带负电荷的浓度大于阳离子所带正电荷的浓度,故溶液中应含大量氢离子,即溶液显酸性,根据c(H+)+c(Na+)=2c(SO42-)+c(Cl-)带入数据计算出氢离子浓度,再根据pH=-lgc(H+)计算出该溶液的pH;
(2) NH4+发生水解,溶液显示酸性;
(3)根据水的电离和题给信息结合外界条件对平衡移动的影响分析。
(1)任何溶液中均满足电荷守恒,因为测得Na+、SO42-和Cl-三种离子的浓度分别是0.01 mol·L-1、0.0035 mol·L-1和0.004 mol·L-1,溶液中的阴离子所带负电荷的浓度大于阳离子所带正电荷的浓度,故溶液中应含大量氢离子,即溶液显酸性,
根据电荷守恒c(H+)+c(Na+)=2c(SO42-)+c(Cl-)可以知道溶液中氢离子浓度为:c(H+)=0.0035mol/L×2+0.004mol/L-0.01mol/L=0.001mol/L,
该溶液的pH=-lgc(H+)=-lg10-3=3,
因此,本题正确答案是:3;
(2) NH4Cl溶液中NH4+部分水解,显酸性,水解离子反应为: NH4++H2O![]() NH3·H2O+H+,
NH3·H2O+H+,
因此,本题正确答案是:NH4++H2O![]() NH3·H2O+H+;
NH3·H2O+H+;
(3)液氨类似于水的电离,已知水的电离方程式可写为2H2OH3O++OH-,则液氨的电离方程式为2NH3NH4++NH2-,在液氨中加入NH4Cl,NH4+浓度增大,则平衡向逆反应方向移动,
因此,本题正确答案是:2NH3NH4++NH2-;逆反应方向。


科目:高中化学 来源: 题型:
【题目】一定条件下,对于可逆反应X(g)+3Y(g) ![]() 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.12 mol/L,则下列判断正确的是
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.12 mol/L,则下列判断正确的是
A. c1 : c2=1 : 3 B. 平衡时,3υY (正) =2υZ (逆)
C. X、Y的转化率不相等 D. c1的取值范围为0.06<c1<0.16 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,将潮湿的![]() 通过甲装置后再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂不可能是
通过甲装置后再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂不可能是

A.饱和食盐水B.浓硫酸C.KI溶液D.NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是一种常见的强氧化剂,主要用于防腐、化工、制药等。现以某种软锰矿
是一种常见的强氧化剂,主要用于防腐、化工、制药等。现以某种软锰矿![]() 主要成分
主要成分![]() ,还有
,还有![]() 、
、![]() 、
、![]() 等
等![]() 作脱硫剂,通过如下简化流程既脱除燃煤尾气中的
作脱硫剂,通过如下简化流程既脱除燃煤尾气中的![]() ,又制得
,又制得![]() 反应条件已经省略
反应条件已经省略![]() 。
。
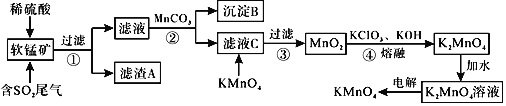
已知:![]() ,
,![]() 回答下列问题:
回答下列问题:
![]() 滤渣A的成分是
滤渣A的成分是![]() 写化学式
写化学式![]() ______。
______。
![]() 析出沉淀B时,首先析出的物质是
析出沉淀B时,首先析出的物质是![]() 写化学式
写化学式![]() ______。
______。
![]() 步骤2中加入
步骤2中加入![]() 的作用为______。
的作用为______。
![]() 滤液C中加入
滤液C中加入![]() 时发生反应的离子方程式是______。
时发生反应的离子方程式是______。
![]() 完成步骤4中反应的化学方程式______
完成步骤4中反应的化学方程式______![]() ______
______![]() ______
______![]() ______
______
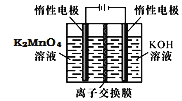
![]() 电解制备
电解制备![]() 的装置如图所示。电解液中最好选择______离子交换膜
的装置如图所示。电解液中最好选择______离子交换膜![]() 填“阳”或“阴”
填“阳”或“阴”![]() 。电解时,阳极的电极反应式为______。
。电解时,阳极的电极反应式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用纯净干燥的氯气通过如下装置与铁反应。(已知:氯气与铁的产物具有很强的吸湿性,应避免接触潮湿空气。)
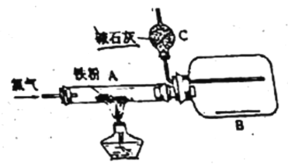
(1)当纯净干燥的氯气通过灼热铁粉时,可以看到装置A内产生_______,A中发生反应的化学方程式为:_______________。
(2)产物用氯气赶入装置B中冷却收集,推测装置C的作用是_______。
a.吸收多余的氯气 b.吸收空气中的水蒸气
c.吸收空气中的二氧化碳 d.吸收生成的氯化氢
(3)实验前需要用氯气排出装置内原有的空气,请给出一种简易判断装置内已充满氯气的方法__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25 ℃、101 kPa下,1 g C8H18(辛烷)燃烧生成二氧化碳和液态水放出48.40 kJ热量,表示上述反应的热化学方程式正确的是( )
A. C8H18(l) + O2(g)![]() 8CO2(g) + 9H2O(l) ΔH=-48.40 kJ·mol-1
8CO2(g) + 9H2O(l) ΔH=-48.40 kJ·mol-1
B. C8H18(l) + O2(g)![]() 8CO2(g) + 9H2O(l) ΔH=-5 518 kJ·mol-1
8CO2(g) + 9H2O(l) ΔH=-5 518 kJ·mol-1
C. C8H18(l) + O2(g)![]() 8CO2(g) + 9H2O(l) ΔH=+5 518 kJ·mol-1
8CO2(g) + 9H2O(l) ΔH=+5 518 kJ·mol-1
D. C8H18(l) + O2(g)![]() 8CO2(g) + 9H2O(l) ΔH=+48.40 kJ·mol-1
8CO2(g) + 9H2O(l) ΔH=+48.40 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素在生物体内的含量分布情况,下列表述不正确的是( )

A.I在非生物界中都能找到,体现了生物界与非生物界的统一性
B.Ⅱ含量虽少,但却是生物体正常生命活动不可缺少的
C.Ⅱ和Ⅲ称为必需元素,一旦缺乏就可能会导致相应的病症
D.P、S、K 、B、Ca、属于大量元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用纯净的CaCO3与l00mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积己折算为标准状况下的体积)。下列分析正确的是

A. EF段,用盐酸表示该反应的平均反应速率为0.4mol/(L·min)
B. OE段表示的平均速率最快
C. OE、EF、FG三段中,该反应用二氧化碳表示的平均反应速率之比为2:6:7
D. F点收集到的CO2的量最多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环之间共用一个碳原子的化合物称为螺环化合物,氧杂螺戊烷的结构简式为![]() ,则下列说法正确的是
,则下列说法正确的是
A. lmol该有机物完全燃烧需要消耗5.5molO2
B. 二氯代物超过3种
C. 该有机物与环氧乙烷互为同系物
D. 该有机物所有碳、氧原子处于同一平面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com