
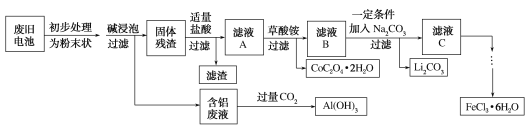
ЎѕМвДїЎїоЬЛбп®ЈЁLiCoO2Ј©µзіШКЗТ»ЦЦУ¦УГ№г·єµДРВРНµзФґЈ¬µзіШЦРє¬УРЙЩБїµДВБЎўМъЎўМјµИµҐЦКЎЈКµСйКТіўКФ¶Ф·ПѕЙоЬЛбп®µзіШ»ШКХФЩАыУГЎЈКµСй№эіМИзПВЈє
ТСЦЄЈєўЩ»№ФРФЈєClЈ>Co2Ј«Ј»
ўЪFe3Ј«єН![]() ЅбєПЙъіЙЅПОИ¶ЁµД[FeЈЁC2O4Ј©3]3ЈЈ¬ФЪЗїЛбРФМхјюПВ·ЦЅвЦШРВЙъіЙFe3Ј«ЎЈ»ШґрПВБРОКМвЈє
ЅбєПЙъіЙЅПОИ¶ЁµД[FeЈЁC2O4Ј©3]3ЈЈ¬ФЪЗїЛбРФМхјюПВ·ЦЅвЦШРВЙъіЙFe3Ј«ЎЈ»ШґрПВБРОКМвЈє
ЈЁ1Ј©·ПѕЙµзіШіхІЅґ¦АнОЄ·ЫД©ЧґµДДїµДКЗ________ЎЈ
ЈЁ2Ј©ґУє¬ВБ·ПТєµГµЅAlЈЁOHЈ©3µДАлЧУ·ЅіМКЅОЄ___________
ЈЁ3Ј©ВЛТєAЦРµДИЬЦКіэHClЎўLiClНв»№УР________ЈЁМо»ЇС§КЅЈ©ЎЈРґіцLiCoO2єНСОЛб·ґУ¦µД»ЇС§·ЅіМКЅ____________
ЈЁ4Ј©ВЛФьµДЦчТЄіЙ·ЦОЄ_______ЈЁМо»ЇС§КЅЈ©ЎЈ
ЈЁ5Ј©ФЪїХЖшЦРјУИИТ»¶ЁЦКБїµДCoC2O4Ў¤2H2O№ММеСщЖ·К±Ј¬Жд№ММеК§ЦШВККэѕЭјыПВ±нЈ¬ЗлІ№ідНкХы±нЦРОКМвЎЈ
ТСЦЄЈєўЩCoC2O4ФЪїХЖшЦРјУИИК±µДЖшМеІъОпОЄCO2ЎЈ
ўЪ№ММеК§ЦШВКЈЅ¶ФУ¦ОВ¶ИПВСщЖ·К§ЦШµДЦКБї/СщЖ·µДіхКјЦКБїЎЈ
РтєЕ | ОВ¶И·¶О§/Ўж | »ЇС§·ЅіМКЅ | №ММеК§ЦШВК |
ўс | 120Ў«220 | CoC2O4Ў¤2H2O CoC2O4Ј«2H2O | 19.67% |
ўт | 300Ў«350 | ______ | 59.02% |
ЈЁ6Ј©ТСЦЄLi2CO3µДИЬ¶И»эіЈКэKspЈЅ8.64ЎБ10Ј4Ј¬Ѕ«ЕЁ¶ИОЄ0.02 molЎ¤LЈ1µДLi2SO4єНЕЁ¶ИОЄ0.02 molЎ¤LЈ1µДNa2CO3ИЬТєµИМе»э»мєПЈ¬ФтИЬТєЦРµДLiЈ«ЕЁ¶ИОЄ________ molЎ¤LЈ1ЎЈ
Ўѕґр°ёЎїФцґуЅУґҐГж»эЈ¬јУїм·ґУ¦ЛЩВКЈ¬МбёЯЅюіцВК AlO2-Ј«CO2Ј«2H2O=AlЈЁOHЈ©3ЎэЈ«HCO3- FeCl3ЎўCoCl2 2LiCoO2Ј«8HCl=2CoCl2Ј«Cl2ЎьЈ«4H2OЈ«2LiCl C 2CoC2O4Ј«O2![]() 2CoOЈ« 4CO2 0.02
2CoOЈ« 4CO2 0.02
ЎѕЅвОцЎї
(1)ґУ·ґУ¦ОпіК·ЫД©ЧґЅУґҐГж»эј«ґу¶Ф·ґУ¦µДУ°ПмАґ»ШґрЈ»
(2)БчіМНјЦЄє¬ВБ·ПТєіКјоРФЈ¬ТтґЛКЗЖ«ВБЛбёщИЬТєЦРНЁ№эБї¶юСх»ЇМјЈ¬РґµГµЅAlЈЁOHЈ©3µДАлЧУ·ЅіМКЅЈ»
(3)ВЛТєAµДіЙ·ЦЈ¬ґУµзіШЛщє¬µДОпЦКУлHCl·ґУ¦Аґ»ШґрЈ¬µ±И»ТЄЕЕіэТСЧЄТЖµЅјоТєЦРµДВБФЄЛШЈ» LiCoO2єНСОЛб·ґУ¦µД»ЇС§·ЅіМКЅЈ¬ЅбєПРЕПўЕР¶ПКЗСх»Ї»№Ф·ґУ¦Ј¬°ґСх»Ї»№Ф·ґУ¦№жВЙКйРґЈ»
(4)ВЛФьµДЦчТЄіЙ·ЦОЄ·ПµзіШЧЬјИІ»ИЬУЪЛбУЦІ»ИЬУЪјоµДіЙ·ЦЈ»
(5) І№ідНкХы±нЦРОКМвЈ¬ТЄґУЛщМṩµДРЕПўЎўКэѕЭЈ¬ЅбєПФЄЛШЦКБїКШєг¶ЁВЙјЖЛгµГіцЈ»
(6)АлЧУЕЁ¶ИµДјЖЛгЈ¬ПИТЄУГЕЁ¶ИКЗєНKSPµД№ШПµЕР¶ПКЗ·сУРМјЛбп®іБµнЈ¬ИзУРіБµнЈ¬ЅбєПКэѕЭјЖЛгЈ¬ИзГ»УРіБµнЈ¬ФтѕНКЗ»мєПИЬТєЦРАлЧУµДЕЁ¶ИЈ»
·ПѕЙоЬЛбп®ДшАлЧУµзіШЦчТЄє¬УРFeЎўAlЎўМјµДµҐЦКєНLiCoO2Ј¬іхІЅґ¦АнЈ¬јУјоЅюЕЭЈ¬ВБєНјоТє·ґУ¦ЙъіЙЖ«ВБЛбСОєНЗвЖшЈ¬№ММеІРФьОЄЈєFeЎўCµДµҐЦКєНLiCoO2Ј¬јУСОЛбFe+2H+=Fe2++H2ЎьЈ¬2LiCoO2+8H++2Cl-=2Li++2Co2++Cl2Ўь+4H2OЈ¬ІРФьОЄCЈ¬ВЛТєAОЄFe3+ЎўLi+ЎўCo3+ЎўCl-Ј¬јУИлІЭЛбп§Ј¬№эВЛіБµнОЄCoC2O42H2OЈ¬ВЛТєBОЄЈєFe3+ЎўLi+ЎўCl-Ј¬јУИлМјЛбДЖЈ¬·ўЙъµДАлЧУ·ґУ¦ОЄ2Li++CO32-=Li2CO3ЎэЈ¬ВЛТєCОЄFe3+ЎўCl-Ј¬јУИлСх»ЇјБ·АЦ№МъАлЧУ±»»№ФЈ¬µГВИ»ЇМъИЬТєЈ»
(1)·ПѕЙµзіШіхІЅґ¦АнОЄ·ЫД©ЧґµДДїµДКЗЈєФцґуЅУґҐГж»эЈ¬јУїм·ґУ¦ЛЩВКЈ¬МбёЯЅюіцВКЈ»
ґр°ёОЄЈєФцґуЅУґҐГж»эЈ¬јУїм·ґУ¦ЛЩВКЈ¬МбёЯЅюіцВКЈ»
(2) Ж«ВБЛбДЖИЬТєЦРНЁИл№эБї¶юСх»ЇМј·ґУ¦ЙъіЙЗвСх»ЇВБіБµнєНМјЛбЗвДЖЈ¬ТтґЛґУє¬ВБ·ПТєµГµЅAl(OH)3µДАлЧУ·ґУ¦·ЅіМКЅОЄЈєAlO2-Ј«CO2Ј«2H2O=AlЈЁOHЈ©3ЎэЈ«HCO3-Ј»
ґр°ёОЄЈєAlO2-Ј«CO2Ј«2H2O=AlЈЁOHЈ©3ЎэЈ«HCO3-Ј»
(3) LiCoO2ЦРLiОЄ+1јЫЈ¬CoОЄ+3јЫЈ¬ѕЯУРСх»ЇРФЈ¬HClЦР-1јЫµДВИѕЯУР»№ФРФЈ¬Пт№ММеІРФьЦРјУИлСОЛбК±Ј¬·ўЙъСх»Ї»№Ф·ґУ¦Ј¬CoЈЁ+3Ўъ+2Ј©Ј¬ClЈЁ-1Ўъ0Ј©Ј¬·ґУ¦±нКѕОЄЈє2LiCoO2+8H++2Cl-=2Li++2Co2++Cl2Ўь+4H2O»т2LiCoO2Ј«8HCl=2CoCl2Ј«Cl2ЎьЈ«4H2OЈ«2LiClЈ»Ј¬ВЛТєAОЄFe3+ЎўLi+ЎўCo3+ЎўCl-Ј¬№КВЛТєAЦРµДИЬЦКОЄHClЎўLiClЎўFeCl3ЎўCoCl2Ј»
ґр°ёОЄЈєFeCl3ЎўCoCl2Ј»2LiCoO2Ј«8HCl=2CoCl2Ј«Cl2ЎьЈ«4H2OЈ«2LiClЈ»
(4)ЙПКц·ЦОцїЙЦЄЈ¬ВЛФьµДЦчТЄіЙ·ЦОЄCЈ»
ґр°ёОЄЈєCЈ»
(5) ФЪїХЖшЦРјУИИТ»¶ЁЦКБїµДCoC2O4Ў¤2H2O№ММеСщЖ·К±Ј¬КЧПИК§ИҐЅбѕ§Л®Ј¬ФЪ120Ў«220ЎжК±Ј¬№ММеК§ЦШВКОЄ19.76%Ј¬ЙъіЙІъОпОЄCoC2O4Ј»
УЙўЩїЙЦЄЈ¬ФЪ120Ў«220ЎжК±Ј¬CoC2O4Ў¤2H2OНкИ«К§ИҐЅбѕ§Л®ЙъіЙCoC2O4Ј¬И»єујМРшЙэёЯОВ¶ИјУИИЈ¬ФтCoC2O4·ЦЅвЙъіЙСх»ЇОпЈ¬Жд·ЦЅвК§ИҐµДЦКБїОЄ183gЎБ59.02%=108gЈ¬КЈУаµДЦКБїОЄ183g-108g=75gЈ¬ЙиІъОпµД»ЇС§КЅОЄCoOxЈ¬Фт59+16x=75Ј¬ЅвµГx=1Ј¬Фт»ЇС§КЅОЄCoOЈ¬Фт·ґУ¦·ЅіМКЅОЄЈє2CoC2O4Ј«O2![]() 2CoOЈ« 4CO2Ј»
2CoOЈ« 4CO2Ј»
ґр°ёОЄЈє2CoC2O4Ј«O2![]() 2CoOЈ« 4CO2Ј»
2CoOЈ« 4CO2Ј»
(6) Ѕ«ЕЁ¶ИОЄ0.02molL-1µДLi2SO4єНЕЁ¶ИОЄ0.02molL-1µДNa2CO3ИЬТєµИМе»э»мєПЈ¬»мєПЛІјдИЬТєЦРc(Li+) =0.02mol/LЈ¬c(CO32-) =0.01mol/LЈ¬јЖЛгЕЁ¶ИЙМ![]() =4ЎБ10-6<Ksp=8.64ЎБ10-4Ј¬ОЮіБµнЙъіЙЈ¬ФтґЛК±ИЬТєЦРLi+ЕЁ¶ИОЄ0.02mol/LЈ»
=4ЎБ10-6<Ksp=8.64ЎБ10-4Ј¬ОЮіБµнЙъіЙЈ¬ФтґЛК±ИЬТєЦРLi+ЕЁ¶ИОЄ0.02mol/LЈ»
ґр°ёОЄЈє0.02ЎЈ


 їЪЛгМвїЁјУУ¦УГМвјЇСµПµБРґр°ё
їЪЛгМвїЁјУУ¦УГМвјЇСµПµБРґр°ё
| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїКµСйРЎЧйАыУГґ«ёРЖчМЅѕїNa2CO3єНNaHCO3µДРФЦКЎЈ
КµСйІЩЧч | КµСйКэѕЭ |
ІвБїПВКцКµСй№эіМµДpH±д»Ї
|
|
ПВБР·ЦОцІ»ХэИ·µДКЗ
A.ўЩУлўЪµДКµСйКэѕЭ»щ±ѕПаН¬Ј¬ЛµГчўЪЦРµДOHЈОґІОУлёГ·ґУ¦
B.јУИлКФјБМе»эПаН¬К±Ј¬ўЪЛщµГіБµнЦКБїґуУЪўЫЛщµГіБµнЦКБї
C.ґУЖрКјµЅaµг№эіМЦР·ґУ¦µДАлЧУ·ЅіМКЅОЄЈєCa2Ј«Ј«2OHЈЈ«2HCO3ЈЈЅCaCO3ЎэЈ«2H2OЈ«CO32Ј
D.bµг¶ФУ¦ИЬТєЦРЛ®µДµзАліМ¶ИРЎУЪcµг¶ФУ¦ИЬТєЦРЛ®µДµзАліМ¶И
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїДтЛШ(![]() )µЄФЧУЙПµДЗвФЧУїЙТФПс±Ѕ·У·ЦЧУЦР±Ѕ»·ЙПµДЗвФЧУДЗСщУлјЧИ©·ўЙъ·ґУ¦Ј¬ЙъіЙЅ»БЄлеИ©КчЦ¬Ј¬ЖдЅб№№Ж¬¶ОИзПВНјЛщКѕ(НјЦР ±нКѕБґСУі¤)ЎЈ
)µЄФЧУЙПµДЗвФЧУїЙТФПс±Ѕ·У·ЦЧУЦР±Ѕ»·ЙПµДЗвФЧУДЗСщУлјЧИ©·ўЙъ·ґУ¦Ј¬ЙъіЙЅ»БЄлеИ©КчЦ¬Ј¬ЖдЅб№№Ж¬¶ОИзПВНјЛщКѕ(НјЦР ±нКѕБґСУі¤)ЎЈ

ПВБРЛµ·ЁІ»ХэИ·µДКЗ
A.ДтЛШїЙТФУлјЧИ©·ўЙъјУіЙ·ґУ¦ЙъіЙ ![]()
B.леИ©КчЦ¬µДєПіЙ·ґУ¦ОЄЛхѕЫ·ґУ¦
C.Ѕ»БЄлеИ©КчЦ¬ФЪТ»¶ЁМхјюПВїЙТФ·ўЙъЛ®Ѕв·ґУ¦Ј¬ЦШРВЙъіЙДтЛШєНјЧИ©
D.јЧИ©їЙТФУл![]() Ѕ»БЄіЙНшЧґЅб№№µДлеИ©КчЦ¬
Ѕ»БЄіЙНшЧґЅб№№µДлеИ©КчЦ¬
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї№ШУЪЕЁ¶ИѕщОЄ0.1 mol/LµДИэЦЦИЬТєЈєўЩ°±Л®ЎўўЪСОЛбЎўўЫВИ»Їп§ИЬТєЈ¬ПВБРЛµ·ЁІ»ХэИ·µДКЗ
A. cЈЁNH+4Ј©ЈєўЫЈѕўЩB. Л®µзАліцµДcЈЁH+Ј©ЈєўЪЈѕўЩC. ўЩєНўЪµИМе»э»мєПєуµДИЬТєЈєcЈЁH+Ј©ЈЅc(OH![]() )+c(NH3Ў¤H2O) D. ўЩєНўЫµИМе»э»мєПєуµДИЬТєЈєcЈЁNH+4Ј©Јѕc(Cl
)+c(NH3Ў¤H2O) D. ўЩєНўЫµИМе»э»мєПєуµДИЬТєЈєcЈЁNH+4Ј©Јѕc(Cl![]() )Јѕc(OH
)Јѕc(OH![]() )Јѕc(H+)
)Јѕc(H+)
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїємЖПМСѕЖГЬ·вґўґжК±јдФЅі¤Ј¬ЦКБїФЅєГЈ¬ФТтЦ®Т»КЗґўґж№эіМЦРЙъіЙБЛУРПгО¶µДхҐЎЈФЪКµСйКТТІїЙТФУГИзНјЛщКѕµДЧ°ЦГЦЖИЎТТЛбТТхҐЈ¬Зл»ШґрПВБРОКМвЎЈ
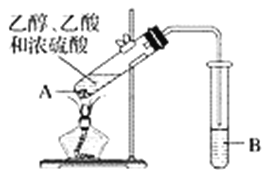
ЈЁ1Ј©КФ№ЬA»мєПИЬТєµДјУИлЛіРтКЗ__________________________________ЎЈ
ЈЁ2Ј©КФ№ЬAЦРјУИлјёїйЛйґЙЖ¬µДДїµДКЗ______________________ЎЈ
ЈЁ3Ј©КФ№ЬAЦР·ўЙъ·ґУ¦µД»ЇС§·ЅіМКЅОЄ______________Ј¬·ґУ¦АаРНКЗ__________ЎЈ
ЈЁ4Ј©·ґУ¦їЄКјЗ°Ј¬КФ№ЬBЦРКў·ЕµДИЬТєКЗ_______________________ЎЈ
ЈЁ5Ј©КФ№ЬBЦРїЙДЬ№ЫІмµЅµДПЦПуКЗ______________________________ЎЈ
ЈЁ6Ј©Ѕ«КФ№ЬBЦРµДОпЦК·ЦАлµГµЅТТЛбТТхҐЈ¬±ШРлК№УГµДТЗЖчКЗ________Ј¬ѕЯМеІЩЧчКЗЅ«ТТЛбТТхҐґУёГТЗЖчµД________________________(МоЎ°ПВїЪ·ЕіцЎ±»тЎ°ЙПїЪµ№іцЎ±)ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї№ШУЪУР»ъОпa(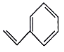 )Ўўb(
)Ўўb(![]() )Ўўc(
)Ўўc(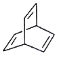 )µДЛµ·ЁґнОуµДКЗ
)µДЛµ·ЁґнОуµДКЗ
A. aЎўbЎўc»ҐОЄН¬·ЦТм№№Ме
B. aЎўcѕщДЬК№ЛбРФёЯГМЛбјШИЬТєНКЙ«
C. aЎўcУлЧгБїЗвЖш·ґУ¦ПыєДЗвЖшµДОпЦКµДБїЦ®±ИКЗ4ЎГ3
D. aЎўbЎўcµДТ»ВИґъОп·Ц±рУР4ЦЦЎў1ЦЦЎў2ЦЦ(І»їјВЗБўМеТм№№)
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїТ»¶ЁОВ¶ИПВµДєгИЭГЬ±ХИЭЖчЦРЈ¬·ґУ¦A2(g)Ј«B2(g)![]() 2AB(g)ґпµЅЖЅєвµД±кЦѕКЗЈЁ Ј©
2AB(g)ґпµЅЖЅєвµД±кЦѕКЗЈЁ Ј©
A. ИЭЖчДЪn(A2):n(B2):n(AB)ЈЅ1:1:2
B. ИЭЖчДЪЖшМеµДГЬ¶ИІ»ЛжК±јд±д»Ї
C. ИЭЖчДЪЖшМеµДЧЬС№ЗїІ»ЛжК±јд±д»Ї
D. µҐО»К±јдДЪЙъіЙ2n mol ABЈ¬Н¬К±ЙъіЙn mol A2
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї±ЅјЧЛбТТхҐКЗЦШТЄµДѕ«Пё»Ї№¤КФјБЈ¬іЈУГУЪЕдЦЖЛ®№ыРНКіУГПгѕ«ЎЈКµСйКТЦЖ±ёБчіМИзНјЈє
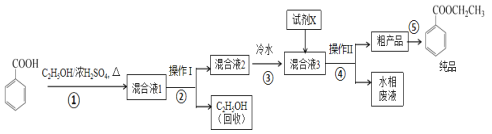
КФјБПа№ШРФЦКИзПВ±нЈє
±ЅјЧЛб | ТТґј | ±ЅјЧЛбТТхҐ | |
іЈОВРФЧґ | °ЧЙ«ХлЧґѕ§Ме | ОЮЙ«ТєМе | ОЮЙ«НёГчТєМе |
·Рµг/Ўж | 249.0 | 78.0 | 212.6 |
Па¶Ф·ЦЧУБї | 122 | 46 | 150 |
ИЬЅвРФ | ОўИЬУЪЛ®Ј¬ТЧИЬУЪТТґјЎўТТГСµИУР»ъИЬјБ | УлЛ®ИОТв±И»ҐИЬ | ДСИЬУЪАдЛ®Ј¬ОўИЬУЪИИЛ®Ј¬ТЧИЬУЪТТґјєНТТГС |
»ШґрПВБРОКМвЈє
(1)ОЄМбёЯФБП±ЅјЧЛбµДґї¶ИЈ¬їЙІЙУГµДґї»Ї·Ѕ·ЁОЄ__ЎЈ
(2)ІЅЦиўЩµДЧ°ЦГИзНјЛщКѕ(јУИИєНјРіЦЧ°ЦГТСВФИҐ)Ј¬Ѕ«Т»РЎНЕГЮ»Ё·ЕИлТЗЖчBЦРїїЅь»оИыїЧґ¦Ј¬Ѕ«ОьЛ®јБ(ОЮЛ®БтЛбНµДТТґј±ҐєНИЬТє)·ЕИлТЗЖчBЦРЈ¬ФЪТЗЖчCЦРјУИл12.2gґї»ЇєуµД±ЅјЧЛбѕ§МеЈ¬30mLОЮЛ®ТТґј(Фј0.5mol)єН3mLЕЁБтЛбЈ¬јУИл·РКЇЈ¬јУИИЦБОў·РЈ¬»ШБч·ґУ¦1.5Ў«2hЎЈТЗЖчAµДЧчУГКЗ__ЎЈ

(3)ЛжЧЕ·ґУ¦ЅшРРЈ¬·ґУ¦МеПµЦРЛ®·ЦІ»¶П±»УРР§·ЦАлЈ¬ТЗЖчBЦРОьЛ®јБµДПЦПуОЄ__ЎЈ
(4)·ґУ¦ЅбКшєуЈ¬¶ФCЦР»мєПТєЅшРР·ЦАлМбґїЈ¬ІЩЧчIКЗ_Ј»ІЩЧчIIЛщУГµДІЈБ§ТЗЖчіэБЛЙХ±Нв»№УР__ЎЈ
(5)·ґУ¦ЅбКшєуЈ¬ІЅЦиўЫЦРЅ«·ґУ¦Тєµ№ИлАдЛ®µДДїµДіэБЛИЬЅвТТґјНвЈ¬»№УР__Ј»јУИлКФјБXОЄ___(МоРґ»ЇС§КЅ)ЎЈ
(6)ЧоЦХµГµЅІъОпґїЖ·10.0gЈ¬КµСйІъВКОЄ__%(±ЈБфИэО»УРР§КэЧЦ)ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїПЦУР¶МЦЬЖЪФЄЛШRЎўXЎўYЎўZЎўTЎЈRУлTФЧУЧоНвІгµзЧУКэѕщКЗµзЧУІгКэµД2±¶Ј»YФЄЛШДЬУлґу¶аКэЅрКфєН·ЗЅрКфФЄЛШРОіЙ»ЇєПОпЈ»Z+УлY2-µзЧУІгЅб№№ПаН¬ЎЈОеЦЦФЄЛШµДФЧУ°лѕ¶УлФЧУРтКэµД№ШПµИзНјЛщКѕЈ¬ПВБРНЖ¶ПХэИ·µДКЗ

A. YЎўZЧйіЙµД»ЇєПОпЦ»є¬АлЧУјь
B. Зв»ЇОпµД·РµгЈєY < X
C. TЎўRµДЧоёЯјЫСх»ЇОп¶ФУ¦µДЛ®»ЇОпµДЛбРФT±ИRµДЗї
D. Y·Ц±рУлTЎўXЧйіЙµД¶юФЄ»ЇєПОпµДЛ®ИЬТєТ»¶ЁКЗЗїЛб
Ійїґґр°ёєНЅвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com