
原子序数依次增大的短周期主族元素W、X、Y、Z和M中,W的最外层电子数为其周期数的二倍;X和Z的A2B型氢化物均为V形分子,Y的+1价离子比M的-1价离子少8个电子,根据以上叙述,下列说法中正确的是( )
A.上述五种元素的原子半径大小为W<X<Y<Z<M
B.由这些元素形成的三原子分子中,空间结构为直线形的有WX2、WZ2、ZX2
C.元素W与氢形成的原子个数比为11的化合物有很多种
D.X与Y可形成含有非极性共价键的共价化合物
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
在一定温度下,某饱和氢氧化钠溶液体积为V mL,溶液密度为d g·cm-3,质量分数为w,物质的量浓度为c mol·L-1,溶液中含氢氧化钠的质量为m g,该温度下NaOH的溶解度为S。
(1)用w来表示该温度下氢氧化钠的溶解度(S)为______________________________。
(2)用c、d来表示该温度下NaOH的溶解度(S)为_____________________________。
(3)用m、V表示溶液中溶质的物质的量浓度(c)为____________________________。
(4)用w、d表示溶液中溶质的物质的量浓度(c)为_____________________________。
(5)用c、d表示溶液中溶质的质量分数(w)为_________________________________。
(6)用S表示溶液中溶质的质量分数(w)为____________________________________。
(7)用S、d表示溶液中溶质的物质的量浓度(c)为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z是1~20号中的四种元素,原子序数依次增大。W的主要化合价为-2,原子半径为0.074 nm;X所在的主族序数与所在的周期序数之差为3;Y原子最外层电子数为奇数;Z最高价氧化物对应的水化物电离出的阴、阳离子数目相等。下列说法正确的是( )
A.W可能是氧元素,也可能是硫元素
B.X元素氧化物对应的水化物一定是一种强酸
C.Y元素原子次外层电子数与最外层电子数之差为1
D.Z可能是氯元素,也可能是钾元素
查看答案和解析>>
科目:高中化学 来源: 题型:
PASS是新一代高效净水剂,它由X、Y、Z、W、R五种短周期元素组成,五种元素原子序数依次增大。X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,电子层数等于主族序数,W单质是人类将太阳能转变为电能的常用材料。下列说法正确的是( )
A.Z与Y形成的化合物可作为耐高温材料
B.WY2能与碱反应,但不能与任何酸反应
C.原子半径按X、Y、Z、R、W的顺序依次增大
D.熔沸点:X2R>X2Y
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F是周期表中短周期的六种元素,有关性质或结构信息如下表:
| 元素 | 有关性质或结构信息 |
| A | 雷雨天大气中会有A的一种单质生成 |
| B | B离子与A离子电子数相同,且是所在周期中单核离子半径最小的 |
| C | C与B同周期,且是所在周期中原子半径最大的(稀有气体除外) |
| D | D是制造黑火药的一种成分,也可用于杀菌消毒 |
| E | E与D同周期,且在该周期中原子半径最小 |
| F | F的简单氢化物和最高价氧化物的水化物反应生成一种离子化合物 |
(1)A与C以原子个数比为1:1形成的化合物的电子式为_______,将0.6 mol该化合物投入到100 mL 3 mol/L BE3溶液中的离子方程式为________________、________________。
(2)F的简单氢化物是由________________(填“极性”或“非极性”)键形成的________________(填“极性”或“非极性”)分子,写出实验室制备该氢化物的化学方程式:________________。
(3)如图实验可用于证明D、E的非金属性的强弱。
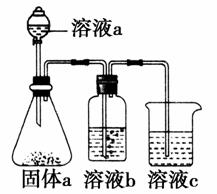
①溶液a和b分别为________________、________________(写化学式)。
②溶液a与固体a反应的离子方程式为________________。
③非金属性D________________E(填“>”或“<”),请从原子结构的角度解释原因:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下下列说法正确的是:( )
A.Na,Mg,Al还原性依次减弱 B.HCl,PH3,H2S稳定性依次减弱
C.NaOH,KOH,CsOH碱性依次减弱 D.S2-,Cl-,Ca2+半径依次增大
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列各元素组中,除一种元素外,其余都可以按某种共性归属一类。请选出各组的例外元素,并将该组其他元素的可能归属按所给6种类型的编号填入表内。
| 元素组 | 例外元素 | 其他元素所属类型编号 |
| ⑴S、N、Na、Mg | ||
| ⑵P、Sb、Sn、As | ||
| ⑶Rb、B、Te、Fe |
归属类型:①主族元素 ②过渡元素 ③同周期元素 ④同族元素 ⑤金属元素 ⑥非金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等。下列判断中,不正确的是
| R | ||
| T | Q | W | |
A.最简单气态氢化物的热稳定性:R>Q
B.最高价氧化物对应水化物的酸性:Q<W
C.原子半径:T>Q>R
D.T元素不可能存在于阴离子中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com