
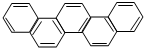
 2015年,北京正在申办冬奥会.有一种有机物因其酷似奥林克五环旗,科学家称其为奥林匹克烃,下列有关奥匹克烃的说中正确的是( )
2015年,北京正在申办冬奥会.有一种有机物因其酷似奥林克五环旗,科学家称其为奥林匹克烃,下列有关奥匹克烃的说中正确的是( )| A. | 该物质属于苯的同系物 | |
| B. | 该物质的一氯代物有一种 | |
| C. | 该物质完全燃烧生成水的物质的量小于二氧化碳的物质的量 | |
| D. | 该物质的分子中只含有非极性键 |
分析 A.苯的同系物中只有苯环一个环状结构;
B.由结构对称性可知,分子中含6种H;
C.由结构可知,分子式为C22H14;
D.该有机物中含C-H键.
解答 解:A.苯的同系物中只有苯环一个环状结构,而该物质含多个苯环,属于芳香族化合物,但不属于苯的同系物,故A错误;
B.由结构对称性可知,分子中含7种H,则该有机物的一氯代物有7种,故B错误;
C.由结构可知,分子式为C22H14,1mol该物质燃烧生成22molCO2,7molH2O,燃烧生成H2O的物质的量小于CO2的物质的量,故C正确;
D.该有机物中含C-H键,则既含极性键又含非极性键,故D错误;
故选C.
点评 本题考查有机物的结构与性质,为高考常见题型,题目难度中等,明确官能团与性质的关系,熟悉燃烧规律及结构对称性即可解答,选项B为解答的难点,试题培养了学生的灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
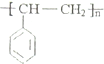 .根据所学知识,可以判断( )
.根据所学知识,可以判断( )| A. | 聚苯乙烯能使溴水褪色 | |
| B. | 聚苯乙烯是一种天然高分子化合物 | |
| C. | 聚苯乙烯可由苯乙烯通过化合反应制得 | |
| D. | 聚苯乙烯单体的分子式为C8H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正极反应式为:O2+2H2O+4e-═4OH- | |
| B. | 工作一段时间后,电解液中KOH的物质的量浓度不变 | |
| C. | 该燃料电池的总反应方程式为O2+2H2═2H2O | |
| D. | 用该燃料电池CuCl2溶液,产生2.24LCl2(标况)时,有0.2mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
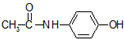 )是最常见的消炎解热镇痛药,用于治疗感冒发烧和关节痛等.M的一种合成路线如下:
)是最常见的消炎解热镇痛药,用于治疗感冒发烧和关节痛等.M的一种合成路线如下:
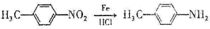 .
. ;
; ;
; ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
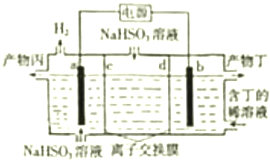
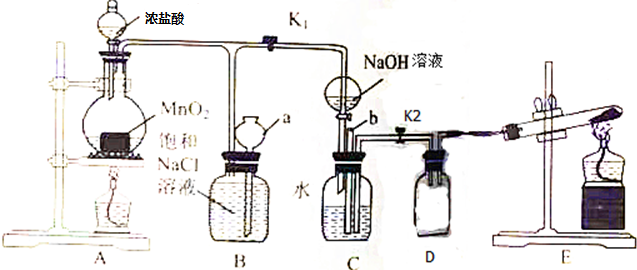
| A. | a极为阴极 | |
| B. | d为阴离子交换膜 | |
| C. | b极反应式为:HSO3-+H2O-2e-═SO42-+3H+ | |
| D. | 产物丙为硫酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④①③② | B. | ①③④② | C. | ①④③② | D. | ①④②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com