
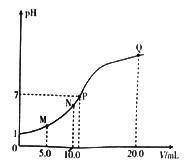
【题目】25℃时,用 0.10 mol·L-1的氨水滴定10.0mL a mol L-1的盐酸,溶液的pH与氨水体积(V)的关系如图所示。已知:N点溶液中存在:c(Cl-)=c(NH4+)+c(NH3·H2O)。下列说法不正确的是
A. a=0.10
B. N、P两点溶液中水的电离程度:N
C. M、N两点溶液中NH4+的物质的量之比大于1:2
D. Q 点溶液中存在:2c(OH-)-2c(H+)=c(NH4+)-c(NH3·H2O)
【答案】B
【解析】A. 加入10mL氨水时溶液显酸性,溶液中存在:c(Cl-)=c(NH4+)+c(NH3·H2O),这说明二者恰好反应生成氯化铵,铵根水解,溶液显酸性,因此a=0.10,A正确;B. N点铵根水解,P点氨水过量,所以溶液中水的电离程度:N>P,B错误;C. M点盐酸过量,抑制铵根水解,则M、N两点溶液中NH4+的物质的量之比大于1:2,C正确;D. Q 点溶液是等浓度的氯化铵和氨水的混合溶液,根据电荷守恒c(OH-)+c(Cl-)=c(NH4+)+c(H+)和物料守恒2c(Cl-)=c(NH4+)+c(NH3·H2O)可知溶液中存在:2c(OH-)-2c(H+)=c(NH4+)-c(NH3·H2O),D正确,答案选B。


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
【题目】2012年4月22日是第43个“世界地球日”,其主题为“绿色梦想,低碳行动”。下列做法符合这一主题的是( ) ①开发太阳能、风能和氢能等能源 ②大量开采地下水,以满足生产、生活的需求 ③使用布袋购物、以步代车等属于“低碳生活”方式 ④开发利用可燃冰是缓解能源紧缺的唯一途径 ⑤利用可降解的“玉米塑料”生产一次性饭盒
A. ①③⑤ B. ①②③ C. ②④⑤ D. ①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请完成下列填空,
(1)已知氢气的化学式是H2,其摩尔质量为______;4 g H2的物质的量为__mol,其标准状况下的体积为_____L,其含H2分子的个数为________.
(2)现有21.6g由CO和CO2组成的混合气体,在标准状况下其体积为13.44L.回答下列问题:
该混合气体的平均摩尔质量为_____________, 该混合气体中含CO2的量为物质的量为__mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烷(C3H8)熔融盐燃料电池和锌蓄电池均为用途广泛的直流电源,放电时二者的总反应分别为C3H8+5O2=3CO2+4H2O,2Zn+O2=2ZnO。用丙烷(C3H8)燃料电池为锌蓄电池充电的装置如图所示,下列说法不正确的是

A. 物质M为CO2
B. 燃料电池消耗1mo1 O2时,理论上有4 mol OH-透过b膜向P电极移动
C. a膜、b膜均适宜选择阴离子交换膜
D. 该装置中,锌蓄电池的负极反应式为Zn+2OH--2e-=ZnO+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1.20 g铁铜合金完全溶于100 mL、12.0 mol·L1浓硝酸中,得到NO2和N2O4混合气体672 mL(换算为标准状况下)。向反应后的溶液中加入1.0 mol·L1 NaOH溶液,当金属离子全部沉淀时,得到2.05 g沉淀。下列有关判断正确的是
A.反应过程中浓硝酸仅体现氧化性
B.该合金中铁与铜物质的量之比是2∶1
C.混合气体中,NO2的体积分数是![]()
D.金属离子全部沉淀时,加入NaOH溶液的体积至少为1100 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳族元素(C、Si、Ge、Sn、Pb)的单质及其化合物在生产和生活中有广泛的应用。回答下列问题:
(1)基态Sn原子中,核外电子占据的最高能级符号为__________,该能级具有的原子轨道数为___________________。
(2)Ge单晶具有晶体硅型结构,Ge单晶的晶体类型为_____________。Ge与同周期的 As、Se相比较,第一电离能由大到小的顺序是_______________。
(3)资料表明,二氧化三碳(C2O2)是金星大气层的一个组成部分,其分子中不含环状结构且每个原子均满足8电子稳定结构。C2O2中碳原子的杂化方式为______________,分子中σ键与π键的个数比为______________________。
(4)碳化硅的晶体结构类似于金刚石(如图所示),1个碳化硅晶胞净占_______个碳原子;二氧化硅晶体中最小环上的原子个数之比为_____________。

(5)石墨可作润滑剂,其主要原因是__________________________。
(6)晶体硅的结构类似于金刚石,已知距离最近的两个硅原子之间的距离为a cm,则硅晶体的密度为_____________g·cm-3(用含有a的代数式表示,用NA表示阿伏伽德罗常数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A. 能使pH试纸变深红色的溶液中:Na+、NH4+、I﹣、NO![]()
B. c(H+)/ c(OH–) = 1×10 -12的溶液中:K+、Na +、CO![]() 、 SO42—
、 SO42—
C. pH=7的溶液中:K+、NH4+、Fe3+、NO![]()
D. 加入铝粉生成H2的溶液:K+、Mg2+、SO![]() 、HCO
、HCO![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com