
| µēĄė³£Źż£Ø25”ę£© |
| HF£ŗ Ka1=3.6”Į10-4 |
| H3PO4£ŗ Ka1=7.5”Į10-3 Ka2=6.2”Į10-8 Ka3=2.2”Į10-13 |
| A”¢ŌŚµČÅØ¶ČµÄNaF”¢NaH2PO4»ģŗĻČÜŅŗÖŠ£¬c£ØNa+£©+c£ØH+£©=c£ØF-£©+c£ØH2PO4-£©+c£ØOH-£© |
| B”¢ÉŁĮæH3PO4ŗĶNaF·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗH3PO4+F-”śH2PO4-+HF |
| C”¢Ķ¬ĪĀĶ¬ÅØ¶ČŹ±£¬ČÜŅŗµÄpH£ŗNaF£¾NaH2PO4£¾Na2HPO4 |
| D”¢½įŗĻH+µÄÄÜĮ¦£ŗPO43-£¾F-£¾HPO42- |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢X2£¾Y2£¾Z2£¾W2 |
| B”¢Y2£¾W2£¾X2£¾Z2 |
| C”¢Z2£¾X2£¾W2£¾Y2 |
| D”¢W2£¾X2£¾Z2£¾Y2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢Ģ¼ĖįøĘÓėĻ”ŃĪĖį·“Ó¦£ŗCO32-+2H+=CO2”ü+H2O |
| B”¢ĢśĘ¬ÓėĀČ»ÆĶČÜŅŗ·“Ó¦£ŗFe+Cu2+=Cu+Fe2+ |
| C”¢ĒāŃõ»ÆĆ¾ČÜÓŚŃĪĖį£ŗMg£ØOH£©2+2H+=Mg2++2H2O |
| D”¢ĢśÓėĻ”ĮņĖį·“Ó¦£ŗ2Fe+6H+=2Fe3++3H2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
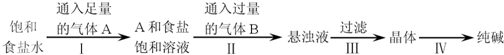
| A”¢AĘųĢåŹĒCO2£¬BĘųĢåŹĒNH3 |
| B”¢µŚ¢ó²½µĆµ½µÄ¾§ĢåŹĒNa2CO3?10H2O |
| C”¢µŚ¢ņ²½µÄĄė×Ó·½³ĢŹ½ĪŖNa++NH3?H2O+CO2ØTNaHCO3”ż+NH4+ |
| D”¢µŚ¢ō²½²Ł×÷µÄÖ÷ŅŖ¹ż³ĢÓŠČܽā”¢Õō·¢”¢½į¾§ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢40mL 1.5 mol?L-1µÄ X ČÜŅŗ |
| B”¢20mL 2 mol?L-1µÄ X ČÜŅŗ |
| C”¢10mL 4 mol?L-1µÄ X ČÜŅŗ |
| D”¢l0mL 2 mol?L-1µÄ X ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
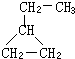 æɱķŹ¾ĪŖ
æɱķŹ¾ĪŖ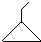 £¬Ōņ½šøÕŅŅĶ锢½šøÕŅŅ°·µÄ½į¹¹¼ņŹ½æÉÓĆĻĀĶ¼±ķŹ¾£®
£¬Ōņ½šøÕŅŅĶ锢½šøÕŅŅ°·µÄ½į¹¹¼ņŹ½æÉÓĆĻĀĶ¼±ķŹ¾£®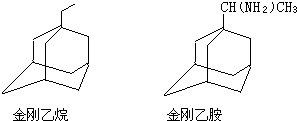
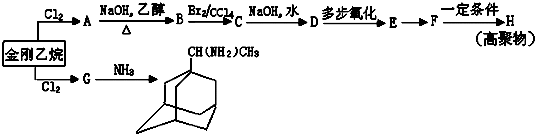
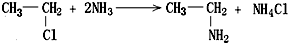
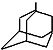 £¬Čē½šøÕŅŅĶé±ķŹ¾ĪŖR-CH2CH3£©
£¬Čē½šøÕŅŅĶé±ķŹ¾ĪŖR-CH2CH3£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ŌŖĖŲ | ÓŠ¹ŲŠŌÖŹ»ņ½į¹¹ŠÅĻ¢ |
| X | »łĢ¬Ō×ÓµÄ×īĶā²ćµē×ÓÅŲ¼Ź½ĪŖnsnnpn |
| Y | Ė«Ō×Ó·Ö×Óµ„ÖŹŌŚ±ź×¼×“æöĻĀĆܶČĪŖ1.429g/L |
| Z | ĖłŌŚÖÜĘŚµÄµ„ŗĖĄė×ÓÖŠ°ė¾¶×īŠ” |
| W | øĆŌŖĖŲŌ×ÓÓŠ1øöĪ“³É¶ŌµÄpµē×Ó |
| T | Ę䵄֏ŗĶŗĻ½š³£ÓĆÓŚŗ½Ģģ¹¤ŅµŗĶŗ½ŗ£¹¤Ņµ£¬Ę䵄֏±»ÓžĪŖ”°21ŹĄ¼Ķ½šŹō”±£¬ĘäŗĖĶāµē×ÓÅŲ¼“ĪĶā²ćµē×ÓŹżŹĒ×īĶā²ćµē×ÓŹżµÄ5±¶ |
| 1 |
| 3 |
| 1 |
| 3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com