
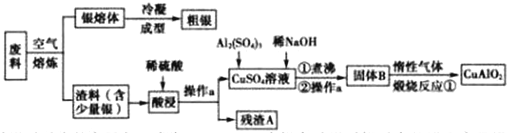
分析 由工艺流程图可知,废料在空气中熔炼时,Cu被氧化,滤渣中含有CuO及少量Ag,向滤渣中加入硫酸进行酸浸,CuO与硫酸反应,过滤得到硫酸铜溶液(含有硫酸),滤渣A为Ag;向滤液中加入硫酸铝、氢氧化钠,得到氢氧化铝、氢氧化铜,灼烧中会得到CuO、Al2O3,二者反应得到CuAlO2.
(1)用硫酸进行酸浸,CuO与硫酸反应生成硫酸铜与水;增大反应物接触面积,能够加快反应速率;
(2)分离固体与液体用到操作为过滤;
(3)依据图中转化关系可知:CuO和Al2O3,灼烧反应生成4CuAlO2和O2;
(4)Ag与稀硝酸反应生成硝酸银、NO与水;为消除污染,应让反应生成的NO、氧气与水反应又得到硝酸,纵观整个过程,Ag失去电子等于氧气获得电子,据此计算氧气物质的量,再计算需要氧气的体积,结合空气中氧气体积分数计算需要空气体积.
解答 解:由工艺流程图可知,废料在空气中熔炼时,Cu被氧化,滤渣中含有CuO及少量Ag,向滤渣中加入硫酸进行酸浸,CuO与硫酸反应,过滤得到硫酸铜溶液(含有硫酸),滤渣A为Ag;向滤液中加入硫酸铝、氢氧化钠,得到氢氧化铝、氢氧化铜,灼烧中会得到CuO、Al2O3,二者反应得到CuAlO2.
(1)CuO与硫酸反应生成硫酸铜与水,反应离子方程式:CuO+2H+=Cu2++H2O;将渣料粉碎,增大接触面积,加快反应速率;
故答案为:CuO+2H+=Cu2++H2O;将渣料粉碎;
(2)操作a是分离互不相溶的液体与固体,应是过滤,故答案为:过滤;
(3)CuO和Al2O3,灼烧反应生成4CuAlO2和O2,方程式为:4CuO+2Al2O3$\frac{\underline{\;高温\;}}{\;}$4CuAlO2+O2↑,故答案为:4CuO+2Al2O3$\frac{\underline{\;高温\;}}{\;}$4CuAlO2+O2↑;
(4)Ag与稀硝酸反应生成硝酸银、NO与水,反应的离子方程式为:3Ag+4H++NO3-=3Ag++NO↑+2H2O;反应生成的NO、氧气与水反应又得到硝酸,纵观整个过程,Ag失去电子等于氧气获得电子,故消耗氧气物质的量为$\frac{bmol×1}{4}$=0.25bmol,标况下需要氧气的体积为0.25bmol×22.4L/mol=5.6bL,需要空气的体积为5.6b L÷20%=28b L,
故答案为:3Ag+4H++NO3-=3Ag++NO↑+2H2O;28b.
点评 本题以从废料中回收银并制备铜化工产品载体,考查化学工艺流程、物质分离提纯、电解原理、氧化还原反应配平与计算,明确流程图中物质之间的转化关系,把握氧化还原反应中电子转移守恒规律是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | NH4Cl溶液加水稀释后,恢复至原温度,pH和KW均增大 | |
| B. | 在NaHCO3溶液中:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) | |
| C. | pH=4的CH3COOH溶液和pH=4的NH4Cl溶液中,c(H+)相等 | |
| D. | 0.1 mol/L 的NaOH溶液和CH3COOH溶液等体积混合,则c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编 号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100mL | 200mL | 300mL | 400mL |
| 剩余金属/g | 18.0g | 9.6g | 0 | 0 |
| NO体积/L(标准状况下) | 2.24L | 4.48L | 6.72L | V |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
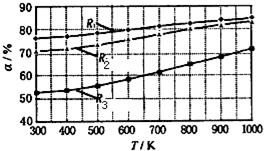 碳酸甲乙酯(CH3OCOOC2H5)是一种理想的锂电池有机电解液.生成碳酸甲乙酯的原理为:C2H5OCOOC2H5(g )+CH3OCOOCH3(g)?2CH3OCOOC2H5(g).其它条件相同时,CH3OCOOCH3的平衡转化率(α)与温度(T)、反应物配比(R=n(C2H3OCOOC2H5):n(CH3OCOOCH3)的关系如图所示.三种反应物配比分别为1:1、2:1、3:1.下列说法不正确的是( )
碳酸甲乙酯(CH3OCOOC2H5)是一种理想的锂电池有机电解液.生成碳酸甲乙酯的原理为:C2H5OCOOC2H5(g )+CH3OCOOCH3(g)?2CH3OCOOC2H5(g).其它条件相同时,CH3OCOOCH3的平衡转化率(α)与温度(T)、反应物配比(R=n(C2H3OCOOC2H5):n(CH3OCOOCH3)的关系如图所示.三种反应物配比分别为1:1、2:1、3:1.下列说法不正确的是( )| A. | 该反应的逆反应△H>0 | |
| B. | 增大反应物中CH3OCOOCH3的浓度能提高碳酸甲乙酯的平衡转化率 | |
| C. | 650℃,反应物配比为1:1时,平衡常数K=6 | |
| D. | 当C2H5OCOOC2H5与CH3OCOOC2H5生成速率比为1:2时,反应达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+先形成沉淀后溶解,后来再形成沉淀接着又沉淀溶解 | |
| B. | 反应后,溶液中NH4+,Fe2+,SO42-的物质的量减少,而Al3+、Cl-的物质的量不变 | |
| C. | Fe2+先被氧化并形成沉淀,后来沉淀溶解并被还原为Fe2+,最后又被氧化 | |
| D. | 该实验中共有两种气体生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com