
【题目】下列说法正确的是
A. 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来说明金属铝的熔点较低
B. 用如图装置进行实验,将装置①中的AlCl3滴入装置②浓氢氧化钠,溶液中可观察到有大量白色沉淀产生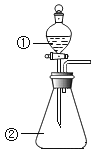
C. Na2O2在空气中久置变白,涉及的氧化还原反应中,Na2O2是还原剂H2O是氧化剂
D. 向明矾溶液里滴加Ba(OH)2溶液,当SO42-恰好完全沉淀时,铝元素几乎全部以AlO2—形式存在于溶液中
【答案】D
【解析】
根据铝及其化合物的性质分析;根据过氧化钠的性质分析;
A.将铝箔用坩埚钳夹住放在酒精灯火焰上加热,铝和氧气反应生成了氧化铝,形成氧化膜,三氧化二铝的熔点高于铝的熔点,包住了熔化的铝,所以加热铝箔的时候铝熔化了但是不会滴落,故A错误;
B.AlCl3滴入浓氢氧化钠溶液中,反应初期NaOH过量,生成NaAlO2,所以没有白色沉淀生成,故B错误;
C.Na2O2在空气中久置变白,涉及的氧化还原反应是Na2O2分别与H2O和CO2反应的过程,这两个反应Na2O2既做氧化剂有作还原剂,故C错误;
D. 向明矾溶液里滴加Ba(OH)2溶液,当SO42-恰好完全沉淀时,KAl(SO4)2与Ba(OH)2以1:2反应,发生的离子反应方程式为:2Ba2++2SO42-+4OH-+Al3+=2BaSO4↓+ AlO2—+2H2O,铝元素几乎全部以AlO2—形式存在于溶液中,故D正确。
故选D。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】过碳酸钠(Na2CO4)是一种很好的供氧剂,其与稀盐酸反应的化学方程式为:2Na2CO4+4HCl=4NaCl+2CO2↑+O2↑+2H2O。市售过碳酸钠一般都含有碳酸钠,为测定某过碳酸钠样品(只含Na2CO4和Na2CO3)的纯度,某化学兴趣小组采用以下两种方案实施:
方案一:[样品] ![]() [样品m1g]
[样品m1g] ![]() [溶液]
[溶液] ![]() [固体]
[固体] ![]() [固体m2g]
[固体m2g]
(1)操作①的名称为___________。
(2)上述操作中,使用到玻璃棒的有________(填操作序号)。
(3)请简述操作③的操作名称_________________。
方案二:按下图安装好实验装置,Q为一塑料气袋,随意取适量样品于其中,打开分液漏斗活塞,将稀盐酸滴入气袋中至充分反应。
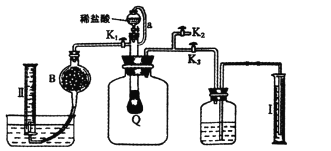
(4)为测定反应生成气体的总体积,滴稀盐酸前必须关闭____,打开_____(填“K1”、“K2”或“K3”)。
(5)当上述反应停止后,使K1、K3处于关闭状态,K2处于打开状态,再缓缓打开K1。B中装的固体试剂是______,为何要缓缓打开K1?__________________。
(6)实验结束时,量筒I中有xmL水,量简II中收集到了ymL气体,则样品中过碳酸钠的质量分数是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知草酸为二元弱酸:
H2C2O4![]() HC2O4-+H+ Ka1
HC2O4-+H+ Ka1
HC2O4-![]() C2O42-+H+ Ka2
C2O42-+H+ Ka2
常温下,向某浓度的草酸溶液中逐滴加入一定量浓度的KOH溶液,所得溶液中H2C2O4、HC2O4-、C2O42-三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的是

A.pH=1.2溶液中:c(K+) + c(H+) = c(OH-) + c(H2C2O4)
B.pH=2.7溶液中:c2(HC2O4-) / [c(H2C2O4) × c(C2O42-)]=1000
C.将相同物质的量KHC2O4和K2C2O4固体完全溶于水可配得pH为4.2的混合液
D.向pH=1.2的溶液中加KOH溶液将pH增大至4.2的过程中水的电离度一直增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿司匹林是一种历史悠久的解热镇痛药,对预防血栓和脑梗有很好的作用, M是一种防晒剂,它们的结构简式分别为:
![]() 和
和![]()
由A出发合成路线如下:

已知:①通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基; ![]()
②![]()
③E能与碳酸氢钠溶液反应产生气体;H能发生银镜反应
根据以上信息回答下列问题
(1)M中含氧官能团的名称____。阿司匹林的核磁共振氢谱中显示有____种不同化学环境的氢原子
(2)写出 H→Ⅰ过程中的反应类型________________。F的结构简式________________。
(3)写出D →E转化过程中①(D + NaOH)的化学方程式________________。
(4)阿司匹林有多种同分异构体,符合下列条件的所有同分异构体有______________种,其中苯环上的一氯代物有两种的结构简式______。(任写出一种)
a.苯环上有3个取代基
b.仅属于酯类,能发生银镜反应,且每摩该物质反应时最多能生成4molAg
(5)写出由Ⅰ到M的合成路线(用流程图表示)。示例
![]() __________________
__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组为了探究Fe(NO3)3的热稳定性和氧化性,设计如下实验:
实验(一): 热稳定性
利用如图装置进行实验,加热A中Fe(NO3)3固体,A 和B中都有红棕色气体产生,A 试管中生成了红色粉末。
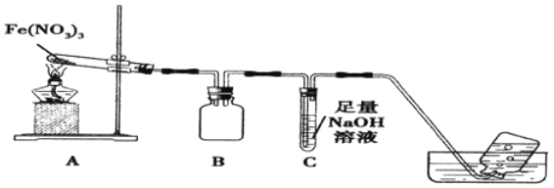
(1)B装置的作用____________;要检验A中红色固体是否为Fe2O3,应该选用的试剂是____________(填化学式)。
(2)加热A中试管一段时间后,C 中导管口有气泡产生,而集气瓶中无气泡产生原因是______________。
(3)写出硝酸铁受热分解的化学方程式__________________。
实验(二):氧化性
Fe3+和Ag+的氧化性相对强弱一直是实验探究的热点。该小组设计如下实验:
试验编号 | 实验操作 | 现象 |
a | 向10mL3mol·L-1KNO3酸性溶液(pH=1)中插入一根洁净的银丝,并滴加氯化钠溶液 | 无沉淀生成 |
b | 向10mL3mol·L-1AgNO3溶液中滴加2mL0.1mol·L-1FeSO4溶液,振荡;再滴加酸性高锰酸钾溶液 | 紫红色溶液不褪色 |
c | 向10 mL3mol·L-1Fe(NO3)3溶液(pH=1)中插入一根洁净的银丝,并滴加氯化钠溶液 | 产生白色沉淀 |
(4)设计实验a的目的是_____________________;实验c的结论是_____________________________。
(5)实验b涉及反应的离子方程式为____________________________________。
(6)实验结论是Fe3+、Ag+氧化性的相对强弱与离子的_____________________有关。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人教版高中化学选修4实验2-3中用到了硫代硫酸钠,某化学兴趣小组对这一物质展开了如下探究。

实验一.制备Na2S2O3·5H2O
通过查阅资料,该化学兴趣小组设计了如下的装置(略去部分夹持仪器)来制取Na2S2O3·5H2O晶体。
已知烧瓶C中发生如下三个反应:
Na2S(aq)+H2O(l)+SO2(g) = Na2SO3(aq)+H2S(aq)
2H2S(aq)+SO2(g) =3S(s)+2H2O(l) ; S(s)+Na2SO3(aq) ![]() Na2S2O3(aq)
Na2S2O3(aq)
(1)写出A中的化学反应方程式___________________________________。
(2)装置B的作用之一是观察SO2的生成速率。控制SO2生成速率可以采取的措施有_________________________(写一条)
(3)装置E的作用是____________________。
(4)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为_________________________。
实验二.性质探究
(5)常温下,用pH试纸测定0.1 mol·L-1 Na2S2O3溶液pH值约为8,测定时的具体操作是_______________________________________________________。
(6)向新制氯水中滴加少量Na2S2O3溶液,氯水颜色变浅,有硫酸根离子生成,写出该反应的离子化学方程式________________________________________。
实验三.Na2S2O3的应用
(7)用Na2S2O3溶液测定废水中Ba2+浓度,步骤如下:取废水25.00 mL,控制适当的酸度加入足量K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解。此时CrO42-全部转化为Cr2O72-;再加过量KI溶液,充分反应后,加入淀粉溶液作指示剂,用0.0100 mol·L-1的Na2S2O3标准溶液进行滴定,反应完全时,相关数据记录如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
消耗Na2S2O3标准溶液的体积/mL | 18.02 | 20.03 | 17.98 | 18.00 |
部分反应的离子方程式为:① Cr2O72-+6I-+14H+===3I2+2Cr3++7H2O
② I2+2S2O32-===S4O62-+2I-
滴定时Na2S2O3标准溶液应该用_____________________(填仪器名称)盛装,该废水中Ba2+的物质的量浓度为_______________________span>。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次增大的短周期主族元素a、b、c、d和e中,a的最外层电子数为其周期数的二倍;b、d 的最简单氢化物为A2B型,且b、d 的最外层电子数之和等于a、c、e的最外层电子数之和,c的+1价离子比e的- 1价离子少8个电子。下列说法正确的是
A. 简单离子的半径:e>d>b>c B. 最高价氧化物对应的水化物的酸性强弱:e>d>a
C. 简单氢化物的沸点:b>d>c D. 简单离子的还原性:b>e>d
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com