
【题目】某试液中只可能含有K+、NH![]() 、Fe2+、Al3+、Cl-、SO
、Fe2+、Al3+、Cl-、SO![]() 、CO
、CO![]() 、AlO
、AlO![]() 中的若干种离子,离子浓度均为0.1mol·L1,某同学进行了如下实验,下列说法正确的是( )
中的若干种离子,离子浓度均为0.1mol·L1,某同学进行了如下实验,下列说法正确的是( )

A.无法确定原试液中是否含有Al3+、Cl-
B.原溶液中存在NH![]() 、Fe2+、Cl-、SO
、Fe2+、Cl-、SO![]()
C.无法确定沉淀C的成分
D.滤液X中大量存在的阳离子有NH![]() 、Fe2+和Ba2+
、Fe2+和Ba2+
【答案】B
【解析】
试液中加入过量稀硫酸,无明显现象,说明无CO32,加入硝酸钡溶液,有气体生成,说明发生了氧化还原反应,则含有Fe2+,则不含AlO2-,有沉淀A,说明沉淀A为硫酸钡沉淀,但不能说明含有SO42,前面加入了硫酸,滤液X加过量NaOH溶液,生成气体,则气体为氨气,则含有NH4+,有沉淀B,说明氢氧化铁沉淀,滤液通入少量二氧化碳,有沉淀C,说明沉淀一定为碳酸钡,可能含氢氧化铝沉淀,则可能含有Al3+,但由于溶液中离子浓度均为0.1mol·L1,结合电荷守恒,因此不可能含有Al3+,一定含有SO42、Cl-、Fe2+、NH4+。
A. 根据分析原试液中一定不含有Al3+,一定含Cl-,故A错误;
B. 根据分析原溶液中存在SO42、Cl-、Fe2+、NH4+,故B正确;
C. 根据分析溶液中不含有Al3+,因此沉淀C为碳酸钡沉淀,故C错误;
D. 滤液X中大量存在的阳离子有NH4+、Fe3+、H+和Ba2+,故D错误;
综上所述,答案为B。


科目:高中化学 来源: 题型:
【题目】过氧化钠可作为氧气的来源。常温常压下二氧化碳和过氧化钠反应后,若固体质量增加了28g,反应中有关物质的物理量正确的是(NA 表示阿伏加德罗常数)
消耗二氧化碳 | 生成碳酸钠 | 转移的电子 | |
A | 1 mol | 2NA | |
B | 22.4 L | 1 mol | |
C | 106 g | 1 mol | |
D | 106 g | 2NA |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇分子结构中各种化学键如图所示,关于乙醇在各种反应中断键的说明不正确的

A.和金属钠反应是键①断裂
B.和浓氢溴酸混合加热时断键②
C.和浓硫酸共热到170℃时断键②和⑤
D.和浓硫酸共热到140℃时仅断键②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2005年诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为①2MoS2+7O2![]() 2MoO3+4SO2;②MoO3+2NH3·H2O====(NH4)2MoO4+H2O;③(NH4)2MoO4+2HCl====H2MoO4↓+2NH4Cl;④H2MoO4
2MoO3+4SO2;②MoO3+2NH3·H2O====(NH4)2MoO4+H2O;③(NH4)2MoO4+2HCl====H2MoO4↓+2NH4Cl;④H2MoO4![]() MoO3+H2O;⑤用还原剂将MoO3还原成金属钼。
MoO3+H2O;⑤用还原剂将MoO3还原成金属钼。
则下列说法正确的是
A. MoS2煅烧产生的尾气可直接排空
B. MoO3是金属氧化物,也是碱性氧化物
C. H2MoO4是一种强酸
D. 利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为3∶3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水的综合利用可以制备金属镁,其流程如下图所示:
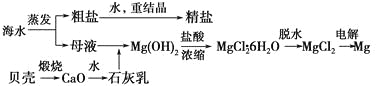
(1)Mg(OH)2沉淀中混有的Ca(OH)2应怎样除去?写出实验步骤。__________________________
(2)实验室将粗盐制成精盐的过程中,溶解、过滤、蒸发三个步骤的操作都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的:
①溶解:________________。
②过滤:__________________________。
③蒸发:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)![]() CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
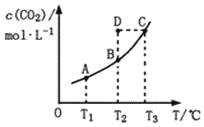
A. 反应CO(g)+H2O(g)![]() CO2(g)+H2(g)的ΔH>0
CO2(g)+H2(g)的ΔH>0
B. 在T2时,若反应处于状态D,则一定有ν正<ν逆
C. 平衡状态A与C相比,平衡状态A的c(CO)小
D. 若T1、T2时的平衡常数分别为K1、K2,则K1<K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以煤为原料可合成一系列燃料。
(1)已知:①2H2(g)+O2(g)= 2H2O(g)△H=-483.6kJ/mol
②CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol
请写出甲醇燃烧生成H2O(g)的热化学方程式_________;
(2)向1L密闭容器中加入2mol CO、4mol H2,在适当的催化剂作用下,发生反应:2CO(g)+4H2(g)![]() CH3OCH3(l)+H2O(l)△H=+71kJ/mol
CH3OCH3(l)+H2O(l)△H=+71kJ/mol
①该反应能否_________自发进行(填“能”、“不能”或“无法判断”)
②下列叙述能说明此反应达到平衡状态的是_________.
a.混合气体的平均相对分子质量保持不变
b.CO和H2的转化率相等
c.CO和H2的体积分数保持不变
d.混合气体的密度保持不变
e.1mol CO生成的同时有1mol O-H键断裂
(3)CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H<0在一定条件下,某反应过程中部分数据如下表:
CH3OH(g)+H2O(g)△H<0在一定条件下,某反应过程中部分数据如下表:
反应条件 | 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
恒温 恒容 (T1℃、 2L) | 0min | 2 | 6 | 0 | 0 |
10min | 4.5 | ||||
20min | 1 | ||||
30min | 1 |
①0~10min内,用H2O(g)表示的化学反应速率v(H20)=_________mol/(L·min)
②达到平衡时,该反应的平衡常数K=_________(用分数表示),平衡时H2的转化率是_________。
③在其它条件不变的情况下,若30min时改变温度为T
(4)用甲醚(CH3OCH3)作为燃料电池的原料,请写出在碱性介质中电池负极反应式_________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等物质的量的PCl5(g)分别放入起始体积相同的恒压容器A和恒容容器B中,相同温度下反应:PCl5(g)![]() PCl3(g)+Cl2(g)达到平衡时,两容器PCl5分解率(用X表示)相比
PCl3(g)+Cl2(g)达到平衡时,两容器PCl5分解率(用X表示)相比
A.XA>XBB.XA<XB
C.XA=XBD.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用固体表面催化工艺进行NO分解的过程如下图所示。下列说法不正确的是
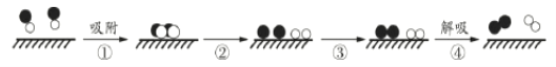
A.该分解过程是:2NO![]() N2+O2
N2+O2
B.实验室制取NO可以用铜与稀硝酸反应
C.过程②释放能量,过程③吸收能量
D.标准状况下,NO分解生成5.6 LN2转移电子数约为6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com