
| A. | R原子的最外层上有4个电子 | |
| B. | RO3n-中的R只能被还原 | |
| C. | HnRO3一定是强酸 | |
| D. | R的单质既具有氧化性又具有还原性 |
分析 由电荷守恒可知,-n+2×(-2)+6×(+1)=0,n=2,RO3n-中元素R的化合价是+4价,R是短周期元素,R2-中元素R的化合价-2价,根据元素周期律,最低负价=主族序数-8,最高正价=其族序数,且有正化合价,所以R是S元素,结合含硫化合物的性质及原子结构来解答.
解答 解:由电荷守恒可知,-n+2×(-2)+6×(+1)=0,n=2,RO3n-中元素R的化合价是+4价,R是短周期元素,R2-中元素R的化合价-2价,根据元素周期律,最低负价=主族序数-8,最高正价=其族序数,且有正化合价,所以R是S元素,
A.最外层上有6个电子,故A错误;
B.RO3n-中元素R的化合价是+4价,中间价态既有氧化性又有还原性,故B错误;
C.R是S元素,亚硫酸是弱酸,故C错误;
D.S的单质化合价居于中间价,既具有氧化性又具有还原性,故D正确.
故选:D.
点评 本题考查氧化还原反应,为高频考点,把握电荷守恒及原子结构与化合价的关系为解答的关键,侧重分析与推断能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 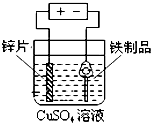 铁制品表面镀锌 | B. | 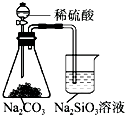 验证碳酸酸性强于硅酸 | ||
| C. | 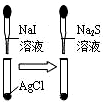 说明溶解性AgCl<AgI<Ag2S | D. |  浸在冷水中的玻璃球颜色较深 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8种 | B. | 16种 | C. | 32种 | D. | 64种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钫与水反应发生爆炸,生成的氢氧化物FrOH是一种极强的碱 | |
| B. | 钫极易在氧气中燃烧,燃烧生成复杂的氧化物 | |
| C. | 砹单质是有色气体,易溶于CCl4等有机溶剂 | |
| D. | 砹单质不容易与氢气化合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铜片(必要时可加热)鉴别浓硝酸、稀硝酸、浓硫酸和浓盐酸 | |
| B. | 将氯化铝溶液加热蒸发、烘干可得无水氯化铝固体 | |
| C. | 用酸式滴定管量取8.00mL1mol/L的KMnO4溶液 | |
| D. | 配制一定浓度的溶液时,若定容时不小心加水超过容量瓶的刻度线,必须重新配制 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 反应的氢气和氧气的总能量高于反应生成的水的总能量 | |
| B. | 2 mol水的总能量高于2 mol氢气和1 mol氧气的总能量 | |
| C. | 断裂2 molH-H键和断裂1 molO═O键吸收的总能量低于形成4 molH-O键放出的总能量 | |
| D. | 断裂4 molH-O键吸收的总能量高于形成2 molH-H键和形成1 molO═O键放出的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ④⑥⑦⑧ | C. | ①④⑥⑦ | D. | ②③⑤⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=1,b=4 | B. | a=3,b=3 | C. | a=2,b=3 | D. | a=3,b=2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com