
����ռ������Ҫ�Ļ���ԭ�ϣ�
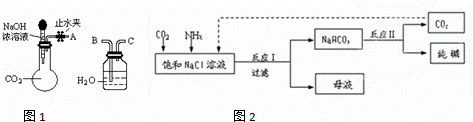
��1��������ͼ1��ʾװ�ÿɼ��֤��������̼���ռ���Һ�����˷�Ӧ����A��B���ӣ���ֹˮ�У�����ͷ�ι��е�Һ�強����ƿ����ʱ��ʵ���������������������������䣬��A��C���ӣ��ɹ۲쵽��������������
��2����100mL 2mol/L��NaOH ��Һ��ͨ��һ����CO2���ᾧ���õ�9.3g��ɫ���壬�ð�ɫ����������������д��ѧʽ����
���ʵ��ȷ�ϸð�ɫ�����д��ڵ������ӣ���������з�����
| ʵ����� | ʵ������ | ���� |
| ��ȡ������ɫ�������Թ��У�������ˮ�ܽ⣬�ټ�����BaCl2��Һ | ||
| �ڹ��ˣ�ȡ2mL��Һ���Թ��� | ||
| �� |
��3���ִ���ҵ�����Ȼ���Ϊԭ���Ʊ�������ֹ���������ͼ2��
��֪NaHCO3�ڵ������ܽ�Ƚ�С����ӦIΪ��NaCl+CO2+NH3+H2O NaHCO3��+NH4Cl������ĸҺ�����ַ������£�
NaHCO3��+NH4Cl������ĸҺ�����ַ������£�
����ĸҺ�м���ʯ���飬�ɽ���������ѭ�����ã�
����ĸҺ��ͨ��NH3������ϸС��ʳ�ο��������£��ɵõ�NH4Cl���壮��д��ͨ��NH3���ܽ�Ƚ�С����ʽ̼����ת��Ϊ�ܽ�Ƚϴ��̼���ε����ӷ���ʽ��������
���㣺
̽��̼������̼�����Ƶ����ʣ��ȼҵ��
ר�⣺
ʵ������⣻Ԫ�ؼ��仯���
������
��1��CO2��NaOH��Ӧ����Na2CO3����ƿ��ѹǿ��С�����жϳ��ֵ�����
��2���ȸ�����ԭ���غ㣬ͨ����ֵ��ȷ����ɫ�������ɣ��������������Լ���Ҫ��������������ҺBaCl2�����̼���ƣ�����̼�������ȫ����������ͨ���������ڵ�pH��ȷ���Ƿ���NaOH��
��1���ٸ������̿�֪��ĸҺ�к����Ȼ�泥�����ʯ�����������ɰ�����
�ڸ��ݰ�ˮ�����笠������������ӣ�����笠���Ũ���������Ȼ�淋���������������Һ������ǿ��ʹ̼������ת��Ϊ�ܽ�Ƚϴ��̼���ƣ�
���
�⣺��1����A��B���ӣ���ֹˮ�У�����ͷ�ι��е�Һ�強����ƿ��������̼���ռ���Һ�����˷�Ӧ������ѹǿ��С������ˮ�ص����ɹ��ƿ������ƿ����Ӧ�����ӷ���ʽΪ2OH﹣+CO2=CO32﹣+H2O����OH﹣+CO2=HCO3﹣�����������������䣬����A��C���ӣ�������������뼯��ƿ���ɹ۲쵽�������ǹ��ƿ�еij����ܿ������ݲ�����
�ʴ�Ϊ��ˮ�ص����ɹ��ƿ������ƿ����ˮ����������ƿ�������ƿ�еij����ܿ������ݲ�����
��2��100mL 2mol/L��NaOH��Һ��ͨ��һ����CO2���ᾧ���õ�9.3g��ɫ���壬�������Ƶ����ʵ���Ϊ��2mol/L��0.1L=0.2mol���������ȫ��Ϊ̼���ƣ���̼���Ƶ�����Ϊ��106g/mol��0.2mol�� =10.6g����ȫ��Ϊ̼�����ƣ���̼�����Ƶ�����Ϊ��84g/mol��0.2mol=16.8g��˵���������ƹ�������ɫ����ΪNaOH��̼�����ƵĻ����������Ȼ��������Ȼ��ƣ���Һ����̼���ƵĴ��ڣ�����ɫ��̪�����������ƵĴ��ڣ�����Ϊ����ȡ������ɫ�������Թ��У�������ˮ�ܽ⣬�ټ�����BaCl2��Һ��������ɫ������˵����Һ�к���̼������ӣ��ڹ��ˣ�ȡ2mL��Һ���Թ��У��۵μӷ�̪����Һ��죬��˵����Һ�к���OH﹣��
=10.6g����ȫ��Ϊ̼�����ƣ���̼�����Ƶ�����Ϊ��84g/mol��0.2mol=16.8g��˵���������ƹ�������ɫ����ΪNaOH��̼�����ƵĻ����������Ȼ��������Ȼ��ƣ���Һ����̼���ƵĴ��ڣ�����ɫ��̪�����������ƵĴ��ڣ�����Ϊ����ȡ������ɫ�������Թ��У�������ˮ�ܽ⣬�ټ�����BaCl2��Һ��������ɫ������˵����Һ�к���̼������ӣ��ڹ��ˣ�ȡ2mL��Һ���Թ��У��۵μӷ�̪����Һ��죬��˵����Һ�к���OH﹣��
�ʴ�Ϊ��NaOH��Na2CO3��
| ʵ����� | ʵ������ | ���� |
| ��﹣﹣ �۵μӷ�̪ | ������ɫ���� ��Һ��� | ��CO32﹣ ��OH﹣ |
��
��3���ٸ������з�Ӧ���̿�֪�����˺�õ���ĸҺ�к����Ȼ�泥�ĸҺ�м���ʯ�����Ӧ���ɰ��������������ڷ�Ӧ������ѭ�����ã��ʴ�Ϊ��NH3��
�ڰ�������ˮ�����ɰ�ˮ����ˮ�����笠������������ӣ�����NH4+��Ũ�ȣ������ڳ���ƽ��������NH4Cl�ķ�����У���Һ������ǿ������NaHCO3ת��ΪNa2CO3������������������Ȼ�淋Ĵ��ȣ���Ӧ�����ӷ���ʽΪHCO3﹣+NH3=NH4++CO32﹣���ʴ�Ϊ��HCO3﹣+NH3=NH4++CO32﹣��
������
���⿼����̼���ơ�̼�����Ƶ����ʡ��ȼҵ�����ʵļ����֪ʶ����Ŀ�Ѷ��еȣ������漰�����ݽ϶࣬ע������̼���ơ�̼�����Ƶ����ʼ����鷽������ȷ�ȼҵԭ�����������ʵļ��顢�ᴿ������
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪3.0g AO32﹣�к������������������6.02��1022��������˵������ȷ���ǣ�������
| �� | A�� | Aԭ�ӵ�Ħ������32g/mol |
| �� | B�� | AO32﹣��Ħ������Ϊ60 |
| �� | C�� | 3.0g AO32﹣ �����ʵ�����0.02mol |
| �� | D�� | AԪ�ص����ԭ������Ϊ12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ϊ�˲ⶨijͭ���Ͻ�ijɷ֣���30.0g�Ͻ�����80ml13.5mol/L��Ũ�����У����Ͻ���ȫ�ܽ���ռ����������6.72L���������Һ��C��H+��=1moL/L�����跴Ӧ����Һ�������Ϊ80mL�����㣺
��1������ԭ����������ʵ�����
��2���Ͻ�����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��������A��NaHCO3��KHCO3��MgCO3��CaCO3���������е����ֻ�϶��ɣ����Ƚ�A���ȣ�ʣ������������������ᷴӦ�����Ⱥ����β���������ֱ�ͨ�������ij���ʯ��ˮ���ɵij�����Ϊ5.0g����A�����ʵ���Ϊ��������
| �� | A�� | 0.10mol | B�� | 0.20mol | C�� | 0.05mol | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��100mL�������ʵ�����HI��H2SO3����Һ��ͨ��0.14molCl2��������֮һ��HI��ΪI2����֪��I2+H2SO3+H2O=4H++SO42﹣+2I﹣����ԭ��Һ��HI��H2SO3��Ũ�ȶ����ڣ�������
| �� | A�� | 8.0mol•L﹣1 | B�� | 0.12mol•L﹣1 | C�� | 0.8mol•L﹣1 | D�� | 1.2mol•L﹣1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���л�ѧ����ʽ����һ�������������ڷ����ϲ�ͬ�������Ӧ�ǣ���
A�� 3Fe+2O2 Fe3O4
Fe3O4
B�� C+CO2 2CO
2CO
C�� NH4HCO3 NH3��+H2O+CO2��
NH3��+H2O+CO2��
D�� Na2CO3+CO2+H2O═2NaHCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ����ȷ���ǣ���
A�� ϡ������NaOH��Һ�ķ�Ӧ��H++OH﹣═H2O
B�� ͭ����ϡ����ķ�Ӧ��Cu+2H+═Cu2++H2��
C�� ������⻯����Һ�ķ�Ӧ��Cl2+I﹣═Cl﹣+I2
D�� ̼������Һ������ϡ����ķ�Ӧ��CO32﹣+2H+═CO2��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�谢���ӵ�����ΪNA������˵����ȷ���ǣ�������
| �� | A�� | 4.4 g��ȩ�����к��еĹ��õ��Ӷ���Ϊ0.6NA |
| �� | B�� | ��״���£�11.2 L���ȼ�������������Ϊ0.5 NA |
| �� | C�� | 18.8 g�����к���̼̼˫���ĸ���Ϊ0.6 NA |
| �� | D�� | ������ϩ����ϩ����ϩ�Ļ�����干14g����ԭ����Ϊ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ڽ���Ԫ�ؼס�����Ԫ�����ڱ��е����λ����ͼ��ʾ�������ж���ȷ���ǣ���
�� ��
�� �� ��
A�� ԭ�Ӱ뾶������������ B�� �����ԣ��ף���
C�� ����������ԣ����������� D�� �������������ף���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com