
用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A. 常温下,14g乙烯和丙烯的混合物中总原子数为3NA个
B. 1mol苯乙烯中含有的碳碳双键数为4NA个
C. 17g羟基(-OH)所含有的电子数是10 NA个
D. 标况下,2.24L苯中含有的碳原子数为0.6NA个
科目:高中化学 来源:2017届辽宁省抚顺市高三3月模拟考试理科综合化学试卷(解析版) 题型:简答题
化学镀镍是指不使用外加电流,利用氧化还原作用在金属制件的表面上沉积一层镍的方法。次磷酸钠(NaH2PO2)是化学镀镍的重要原料,工业上制备NaH2PO2·H2O的流程如下:
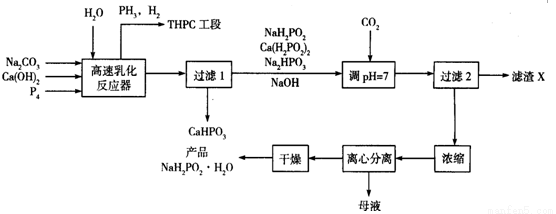
回答下列问题:
⑴次磷酸钠(NaH2PO2)是次磷酸(H3PO2)与足量NaOH溶液反应的产物,NaH2PO2属于_______(填“正盐”“酸式盐”“碱式盐”), NaH2PO2中磷元素的化合价为___________。
(2)在反应器中加入乳化剂并高速搅拌的目的是________________
(3)在反应器中发生多个反应,其中白磷(P4)与Ca(OH)2反应生成次磷酸钠及磷化氢的化学方程式为_________________________
(4)流程中通入CO2的目的是______________,滤渣X的化学式为_____________
(5)流程中母液中的溶质除NaH2PO2外,还有的一种主要成分为_____________
(6)含PH3的废气可用NaClO和NaOH的混合溶液处理将其转化为磷酸盐,该反应的离子方程式为____________
(7)某次生产投入的原料白磷为1240 kg,在高速乳化反应器中有80%的白磷转化为次磷酸钠及磷化氢,忽略其它步骤的损失,理论上最终得到产品NaH2PO2·H2O的质量应为__________kg(NaH2PO2·H2O的相对分子质量为106)
查看答案和解析>>
科目:高中化学 来源:2017届浙江省宁波市高三新高考选考适应性考试化学试卷(解析版) 题型:选择题
下列属于碱的是
A. Na2SO4 B. NaOH C. H2SO4 D. CO2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省四地六校高二下学期第一次联考(3月)化学试卷(解析版) 题型:推断题
下表是关于有机物A、B、C的信息:
A | B | C |
①它的产量可衡量一个国家石油化工发展水平; ②能使溴的四氯化碳溶液褪色; ③可用于果实催熟. | ①C、H两种元素组成 ②分子球棍模型为 | ①分子键线式为 ②相对分子质量为68 |
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称为_______________;
(2)A在一定条件下,与水反应制乙醇的化学方程式:____________________;反应类型是______。
(3)B具有的性质是_____________________(填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大 ⑤任何条件下均不与氢气反应
⑥一定条件下,能与CH2=CH2反应制苯乙烷 ⑦与溴水混合后液体分层且上层呈橙红色
(4)写出B的最简单同系物制TNT的化学方程式 _____________________;反应类型是________。
(5)C是天然橡胶的单体,写出天然高分子橡胶的结构简式________________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省四地六校高二下学期第一次联考(3月)化学试卷(解析版) 题型:选择题
有6种物质:①乙烷;②丙炔;③环己烯;④苯;⑤甲苯;⑥聚乙烯。其中常温下,既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是( )
A. ①③④ B. ①④⑥ C. ①④⑤ D. ②③⑤
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省四地六校高一下学期第一次联考(3月)化学试卷(解析版) 题型:实验题
某同学在实验室研究Fe与H2SO4的反应
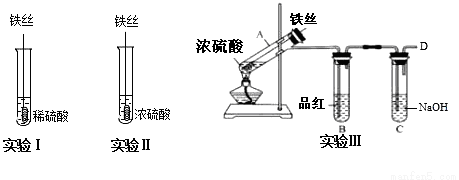
【实验分析】
(1)实验Ⅰ中,铁与稀硫酸反应的离子方程式为__.
(2)实验Ⅱ中,铁丝表面迅速发黑(Fe3O4),有少量气体产生,反应很快停止,
这一现象被称为__.
(3)实验Ⅲ,已知:浓H2SO4的沸点为338.2℃,加热试管A,温度保持在250℃~300℃,产生大量气体,B中品红褪色,D处始终未检测到可燃性气体. A中产生的气体是__,装置C的作用是__.
(4)实验Ⅲ结束后,
甲同学认为装置C中产生Na2SO3,
乙同学认为SO2过量,产物中还可能含有_________,
丙同学认为可能还含有Na2SO4,设计简单实验验证是否含有SO42-,正确的是(____)
A.先加入稀硝酸,没有产生沉淀,然后再加硝酸钡,产生白色沉淀,证明有SO42-存在
B.先加入硝酸钡,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明有SO42-存在
C.先加入稀盐酸,没有产生沉淀,然后再加氯化钡,产生白色沉淀,证明有SO42-存在
(5)对比实验Ⅰ、Ⅱ和Ⅲ,同学们得出以下结论:
①浓硫酸和稀硫酸都具有氧化性,但原因不同,浓硫酸的氧化性源于+6价的S元素,稀硫酸的氧化性源于________.
②影响反应产物多样性的因素有_____________________(至少填两个).
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省四地六校高一下学期第一次联考(3月)化学试卷(解析版) 题型:选择题
现有等体积混合而成的四组气体:①NO2+NO;②NO2+O2;③HCl+N2;④NO+N2,将其分别通入体积相同的试管,并立即倒立于水槽中,试管内水面上升的高度分别为H1,H2,H3,H4,其中高度关系是
A.H2>H3>H1>H4 B.H3>H2>H1>H4
C.H1=H2=H3=H4 D.H1>H2>H3>H4
查看答案和解析>>
科目:高中化学 来源:2017届山东省济宁市高三第一次模拟(3月)理科综合化学试卷(解析版) 题型:实验题
工业上常用亚硝酸钠(NaNO2)作媒染剂、漂白剂、钢材缓蚀剂、金属热处理剂。某兴趣小组用下列装置制备NaNO2并探究NO、NO2的某一化学性质(A中加热装置已略去)。
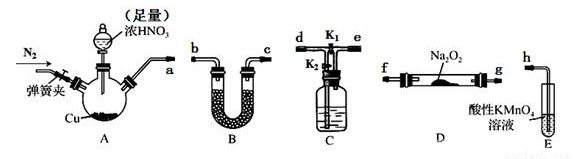
已知:①2NO+Na2O2=2NaNO2;
②NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+
请回答下列问题:
(1)装置A三颈烧瓶中发生反应的化学方程式为__________________。
(2)用上图中的装置制备NaNO2,其连接顺序为:a→_____________→h(按气流方向,用小写字母表示),此时活塞K1、K2如何操作_______________________。
(3)E装置发生反应的离子方程式是________________________。
(4)通过查阅资料,NO2或NO可能与溶液中Fe2+发生反应。某同学选择上述装置并按A→C→E顺序连接,E中装入FeSO4溶液,进行如下实验探究。
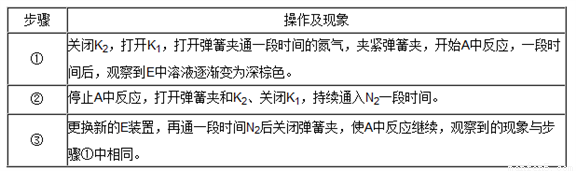
步骤②操作的目的是__________________;步骤③C瓶中发生的化学方程式为________________;
通过实验可以得出:___________(填“NO2、NO中的一种或两种”)和溶液中Fe2+发生反应使溶液呈深棕色。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省益阳市高二下学期3月月考化学试卷(解析版) 题型:填空题
用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖。在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。例如二乙醚的结构简式为:CH3—CH2—O—CH2—CH3。其核磁共振谱中给出的峰值(信号)有两个,如下图(一)所示:
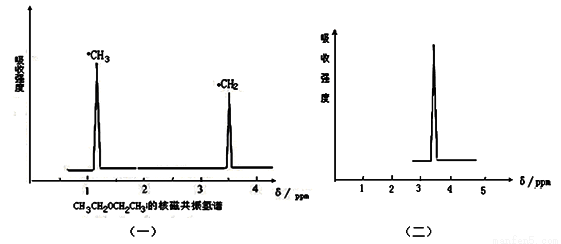
(1)下列物质中,其核磁共振氢谱中给出的峰值(信号)只有一个的是(______);
A.CH3CH3 B.CH3COOH C.CH3COOCH3 D.CH3C(CH3)3
(2)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如上图(二)所示,则A的结构简式为:__________ ,请预测B的核磁共振氢谱上有_______________个峰(信号),强度比为__________;
(3)用核磁共振氢谱的方法来研究C2H6O的结构。若核磁共振氢谱上只有一个峰,则C2H6O的结构简式是__________,若核磁共振氢谱上有三个峰,则C2H6O的键线式是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com