
【题目】纳米材料一直是人们研究的重要课题,例如纳米级Fe粉表面积大,具有超强的磁性,高效催化性等优良的性质。
I、实验室采用气相还原法制备纳米级Fe,其流程如图所示:
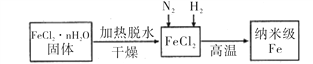
(1)纳米级Fe和稀盐酸反应的离子方程式为_______________________________。
(2)如何将FeCl2·nH2O固体加热脱水制得无水FeCl2 _____________________________________(用简要文字描述)。
(3)生成纳米级Fe的化学方程式为______________________________________。
II、查阅资料:在不同温度下,纳米级Fe粉与水蒸气反应的固体产物不同,温度低于570℃时生成FeO,高于570℃时生成Fe3O4。甲同学用如图甲装置所示进行纳米级Fe粉与水蒸气反应的实验,乙同学用图乙所示的装置进行纳米级Fe粉与水蒸气的反应并验证产物。

(4)甲装置中纳米级Fe粉与水蒸气反应的化学方程式是 ______________________。
(5)甲装置中仪器a的名称为_______________________。
(6)乙同学为探究实验结束后试管内的固体物质成分,进行了下列实验:
实验步骤 | 实验操作 | 实验现象 |
I | 将反应后得到的黑色粉末X(假定为均匀的),取出少量放入另一试管中,加入少量盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
II | 向实验I得到的溶液中滴加几滴KSCN溶液,振荡 | 溶液没有出现红色 |
根据以上实验,乙同学认为该条件下反应的固体产物为FeO。
丙同学认为乙同学的结论不正确,他的理由是______(用简要文字描述)。
(7)丁同学称取5.60gFe粉,用乙装反应一段时间后,停止加热。将试管内的固体物质在干燥器中冷却后,称得质量为6.88g,则丁同学实验后的固体物质中氧化物的质量分数为________(结果保留三位有效数字)。
【答案】 Fe+2H+=Fe2++H2↑ 在干燥的HC1气流中加热 FeCl2+H2![]() Fe+2HCl Fe+H2O(g)
Fe+2HCl Fe+H2O(g)![]() FeO+H2 蒸发皿 加入KSCN溶液,溶液没有出现红色,也可能是因为Fe过量,与生成的Fe3+反应转化为Fe2+ 67.4%
FeO+H2 蒸发皿 加入KSCN溶液,溶液没有出现红色,也可能是因为Fe过量,与生成的Fe3+反应转化为Fe2+ 67.4%
【解析】(1)纳米级Fe和稀盐酸反应生成FeCl2和H2,离子方程式为Fe+2H+=Fe2++H2↑;
(2)FeCl2·nH2O固体加热脱水时,易发生水解,水解方程式为FeCl2+2H2O Fe(OH)2+2HCl,为防止FeCl2水解,在加热脱水时,通常通入干燥的HCl气体,HCl能抑制FeCl2的水解,且通入的HCl气体可带走水蒸气,利于固体脱水。故答案为:在干燥的HC1气流中加热;
(3)根据流程可知,FeCl2·nH2O固体加入脱水得到FeCl2,然后N2、H2与FeCl2在高温条件下反应得到纳米级Fe,反应方程式为FeCl2+H2![]() Fe+2HCl。
Fe+2HCl。
(4)根据已知“纳米级Fe粉与水蒸气反应,温度低于570℃时生成FeO”,甲装置用酒精灯加热,反应温度较低,产物为FeO。Fe失电子,水中H得电子,生成氢气,则反应方程式为Fe+H2O(g) ![]() FeO+H2;
FeO+H2;
(5)仪器a为蒸发皿;
(6)加入KSCN溶液,溶液没有出现红色,说明溶液中没有Fe3+,可能是因为纳米级Fe粉与水蒸气反应的过程中Fe过量,Fe没有反应完;将反应后的固体,加入少量的盐酸,也可能发生反应Fe+2 Fe3+=3Fe2+,所以看不到血红色。
故答案为:加入KSCN溶液,溶液没有出现红色,也可能是因为Fe过量,与生成的Fe3+反应转化为Fe2+;
(7)用乙装置反应,反应温度高于570℃,则Fe粉与水蒸气反应的固体产物为Fe3O4。反应后所得固体的质量为6.88g,其中氧原子的质量为m(O)=6.88g-5.60g=1.28g,则n(O)=![]() =0.08mol。由关系式1 Fe3O4~4 O,可得n(Fe3O4)=0.02mol。所以固体物质中氧化物的质量分数=
=0.08mol。由关系式1 Fe3O4~4 O,可得n(Fe3O4)=0.02mol。所以固体物质中氧化物的质量分数=![]() =
=![]() ≈67.4%
≈67.4%


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ.如图所示,甲、乙两装置电极材料都是铁棒与碳棒,请回答下列问题:
(1)若两装置中均为CuSO4溶液,反应一段时间后:
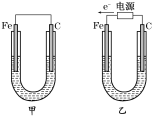
①有红色物质析出的分别是甲、乙装置中的________。
A.甲中的Fe棒,乙中的Fe棒 B.甲中的C棒,乙中的Fe棒
C. 甲中的C 棒,乙中的Fe棒 D.甲中的C棒,乙中的C棒
②乙装置中阳极的电极反应式是:____________________________________________。
(2)若两装置中均为饱和NaCl溶液:
①写出乙装置中总反应的离子方程式:_________________________________________。
②将湿润的淀粉KI试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因:___________。
Ⅱ.如图为绿色电源“甲烷燃料电池”的工作原理示意图。
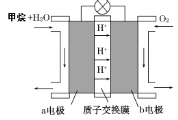
负极的电极反应为______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中有机物化学键断裂只涉及π键断裂的是( )。
A. CH4的燃烧 B. C2H4与Cl2的加成 C. CH4与Cl2的取代 D. C2H4的燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国预计在2020年前后建成自己的载人空间站,为循环利用人体呼出的CO2并提供氧气。我国科学家设计了一种装置(如图所示),实现“太阳能→电能→化学能”转化,总反应为2CO2=2CO+O2,下列有关说法不正确的是
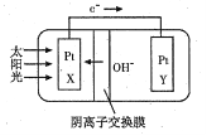
A. 该装置属于电解池
B. X极发生氧化反应,Y极发生还原反应
C. 人体呼出的水蒸气参与Y极反应:CO2+H2O+2e-=CO+2OH-
D. X极每产生标准状况下22.4L气体,有2mol的OH-从Y极移向X极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL 0.0lmol/L CH3COOH 溶液中逐滴加入0.01mol/L的NaOH溶液,溶液中水电离出的c(H+)随加入NaOH溶液的体积变化示意图如图所示,下列说法不正确的是
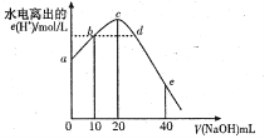
A. 从a到c,醋酸的电离始终受到促进
B. b、d两点溶液的pH相同
C. c点所示溶液中c(Na+)>c(CH3COO- )>c(OH- )>c(H+ )
D. e 点所示溶液中,c(Na+)=2c(CH3COO- )+2c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间。下列说法不正确的是 ( ) 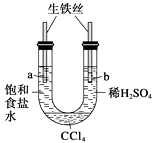
A.a管发生吸氧腐蚀,b管发生析氢腐蚀
B.一段时间后,a管液面高于b管液面
C.a处溶液的pH增大,b处溶液的pH减小
D.a、b两处具有相同的电极反应式:Fe-2e-= Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把下列液体分别装在酸式滴定管中,并使其以细流流下,当用带有静电的玻璃棒接近液体细流时,细流可能发生偏移的是( )
A.CCl4 B.C2H5OH C.CS2 D.C6H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置做铝热反应实验。下列说法不正确的是( )

A.该反应的方程式是2Al+Fe2O3 ![]() 2Fe+Al2O3
2Fe+Al2O3
B.该反应产生高温,发出强光
C.根据铝热反应原理,可以冶炼某些金属
D.若反应中转移3 mol电子,则消耗氧化剂的物质的量是1 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com