
下列方程式正确的是
A.AlCl3 溶液中加入过量氨水:
B.碳酸的电离方程式:
C.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:

D.向Fe(NO3)2稀溶液中加入盐酸:
 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源:2015-2016北京大学附中宇华教育集团高二12月化学卷(解析版) 题型:选择题
用惰性电极电解CuCl2溶液时,如果阴极上有6.4g铜析出,则阳极上产生气体的体积(标准状况)约为( )
A. 2.24L B. 0.56L C. 0.14L D. 1.12L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二上11月月考化学试卷(解析版) 题型:选择题
某有机物的结构简式如右图。下列关于该有机物的叙述正确的是

A.分子中含有3种官能团
B.遇FeCl3溶液呈现为紫色
C.1mol该物质最多可与2molNaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上12月月考化学试卷(解析版) 题型:选择题
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:

下列说法错误的是
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y 2Z,其平衡常数为1600
2Z,其平衡常数为1600
C.增大压强可使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一上12月月考化学试卷(解析版) 题型:选择题
下列有关化学常识正确的是
A.钠钾合金可用于中子反应堆作热交换剂
B.氯气本身有毒,因此不能用于药物合成
C.不用氧化镁电解熔融制镁的原因是氧化镁不导电
D.工业高炉炼铁过程中,加石灰石主要是为了制备还原剂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西省钦南区高一上学期期中质量调研化学试卷(解析版) 题型:选择题
某混合物的水溶液,只可能含有以下离子中的若干:NH4+ 、Cl-、Mg2+、Ba2+、K+、CO32 -、SO42 -,现取三份100 mL溶液进行如下实验:① 第一份加入AgNO3溶液有沉淀产生;② 第二份加足量NaOH溶液加热后,收集到气体0.04 mol;③ 第三份加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥,沉淀质量2.33 g。根据上述实验,以下推测正确的是
A.K+一定不存在 B.该溶液中含CO32 -离子的浓度为0.1 mol/L
C.Cl-可能存在 D.Ba2+一定不存在,Mg2+可能存在
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北航天高中、安陆二中等五校高二上期中化学试卷(解析版) 题型:填空题
A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球。关闭K2,将等量且少量的NO2通过K1、K3分别充入A、B中,反应起始时,A、B的体积相同。(已知:2NO2(g)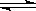 N2O4(g) ΔH<0)
N2O4(g) ΔH<0)
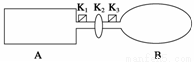
(1)一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是vA__________vB(填“>”、“<”或“=”);若打开活塞K2,气球B将__________(填“变大”、“变小”或“不变”)。
(2)关闭活塞K2,若在A、B中再充入与初始量相等的NO2,则达到平衡时,NO2的转化率αA将____________(填“增大”、“减小”或“不变”);若分别通入等量的氖气,则达到平衡时,A中NO2的转化率将____________,B中NO2的转化率将__________(填“变大”、“变小”或“不变”)。
(3)室温下,若A、B都保持体积不变,将A套上一个绝热层,B与外界可以进行热传递,则达到平衡时,__________中的颜色较深。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上学期期中(理)化学试卷(解析版) 题型:选择题
在2A+B  3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是
A.υ(A)= 0.5 mol/(L·s) B.υ(B)= 18 mol/(L·min)
C.υ(C)= 0.8 mol/(L·s) D.υ(D)= 1 mol/( L·s)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省南昌市高二上学期期中测试化学试卷(解析版) 题型:填空题
(一) A和B反应生成C,假定反应由A、B开始,它们的起始浓度均为1mol/l。反应进行2min后A的浓度为0.8mol/l, B的浓度为0.6mol/l, C的浓度为0.6mol/l。则2min内反应的平均速率为v(A)= ,v (B) = ,v(C)= 。该反应的化学反应方程式为: 。
(二) 比较下列各组热化学方程式中的ΔH的大小关系。
(1)已知1 mol白磷转化成红磷,放出18.39 kJ的热量,又知:①P4 (白,s)+5O2(g)=2P2O5(s) ΔH1,
②4P(红,s)+5O2(g)=2P2O5(s) ΔH2 。
则ΔH1和ΔH2的关系:ΔH1 ΔH2
(2)③ S(g)+O2(g)==SO2(g) △H1
④S(s)+O2(g)==SO2(g) △H2 ΔH1 ΔH2
(3)已知:高温下,在密闭容器中用H2还原WO2可得到金属钨。当温度过高时,WO2(s)会转变为WO2 (g)。请根据以下反应:
⑤WO2 (s) + 2H2 (g)  W (s) + 2H2O (g) ΔH = +66.0 kJ· mol-1
W (s) + 2H2O (g) ΔH = +66.0 kJ· mol-1
⑥WO2 (g) + 2H2  W (s) + 2H2O (g) ΔH = -137.9 kJ· mol-1
W (s) + 2H2O (g) ΔH = -137.9 kJ· mol-1
计算出WO2 (s)  WO2 (g) 的ΔH = ______________________。
WO2 (g) 的ΔH = ______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com